题目内容
【题目】在实验室加热32.5g二氧化锰和氯酸钾的固体混合物制取氧气时,剩余固体物质的质量变化如下图所示。请计算:
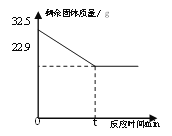
(1)完全反应时,生成氧气的质量为________。
(2)完全反应后,剩余固体物质属_________(填纯净物、混合物)。
(3)原固体混合物中氯酸钾的质量为________(列式计算)。
【答案】 9.6g 混合物 75.4%
【解析】(1)完全反应时,生成氧气的质量为固体减少的质量, ![]() 。
。
(2)加热氯酸钾和二氧化锰的混合物,氯酸钾分解为固体氯化钾和气体氧气,二氧化锰为催化剂,反应前后质量不变,则完全反应后,剩余的固体物质是氯化钾和二氧化锰,属于混合物。
(3)设原固体混合物中氯酸钾的质量为![]() ,则:
,则:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
所以,原固体混合物中氯酸钾的质量为![]() 。
。
答:完全反应时,生成氧气的质量为9.6g;完全反应后,剩余固体物质属于混合物;原固体混合物中氯酸钾的质量为75.4%。

 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案【题目】实验探究一:课本第二单元课后作业中有“寻找新的催化剂” 的探究内容,实验中学探究小组据此设计了如下探究方案。
【提出问题】红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何?
【实验探究】
实验步骤 | 实验现象 | 实验结论及解释 |
Ⅰ. | A中无明显现象, B中产生大量能使带火星木条复燃的气体 | ① 产生的气体是______ ② 红砖粉末能改变过氧化氢分解速率 |
Ⅱ. 向B试管中重新加入5%的过氧化氢溶液,反应停止后过滤、洗涤、干燥、称量滤渣 | ① 又产生大量能使带火星木条复燃的气体 ② 滤渣质量等于ag | 红砖粉末的_____在反应前后均没有发生变化,能作过氧化氢分解的催化剂 |
Ⅲ. | 两试管中均产生气泡且______ | 红砖粉末的催化效果没有二氧化锰粉末好 |
【拓展应用】己知CuSO4也可作为过氧化氢分解的催化剂。写出其反应的符号表达式___________________________