题目内容
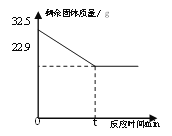
【题目】物质X的化学式为C3H4O6,可发生反应: ![]() 。取136gX,在t℃完全分解,产生H2O 36 g,产生CO2 44 g。则下列说法不正确的是( )
。取136gX,在t℃完全分解,产生H2O 36 g,产生CO2 44 g。则下列说法不正确的是( )
A. 气体Y中一定含有碳、氢、氧三种元素
B. 气体Y的质量为56g
C. 该反应为分解反应
D. 化学方程式中a和b的比为2∶1
【答案】A
【解析】A、由质量守恒定律反应前后元素的种类不变及题意可知,有机物中一定含有碳、氢元素.
136g C3H4O6中氢元素的质量=136g×![]() ×100%═4g,36g水中氢元素的质量=36g×
×100%═4g,36g水中氢元素的质量=36g×![]() ×100%═4g,综合以上述分析可知,136gX中的氢元素反应后全部进入到水中,Y中不再含有氢元素,故气体Y中一定含有碳、氢、氧三种元素是错误的;
×100%═4g,综合以上述分析可知,136gX中的氢元素反应后全部进入到水中,Y中不再含有氢元素,故气体Y中一定含有碳、氢、氧三种元素是错误的;
B、根据质量守恒定律可知气体Y的质量为136g-44g-36g=56g,故正确;
C、 该反应是由一种物质生成三种物质,属于分解反应。故正确;
D、 136g C3H4O6中碳元素的质量136g×![]() ×100%═36g,44g二氧化碳中碳元素的质量=44g×
×100%═36g,44g二氧化碳中碳元素的质量=44g×![]() ×100%═12g,则Y中碳元素的质量为36g-12g=24g;136g C3H4O6中氧元素的质量136g×
×100%═12g,则Y中碳元素的质量为36g-12g=24g;136g C3H4O6中氧元素的质量136g×![]() ×100%═96g,36g水中氢元素的质量=36g×
×100%═96g,36g水中氢元素的质量=36g×![]() ×100%═32g,44g二氧化碳中氧元素的质量=44g×
×100%═32g,44g二氧化碳中氧元素的质量=44g×![]() ×100%═32g,则Y中氧元素质量为96g-32g-32g=32g;Y中碳元素与氧元素的质量比为24g:32g=3:4,所以Y为CO,配平该化学方程式得 a=2b=1故化学方程式中a和b的比为2∶1是正确的,故选A
×100%═32g,则Y中氧元素质量为96g-32g-32g=32g;Y中碳元素与氧元素的质量比为24g:32g=3:4,所以Y为CO,配平该化学方程式得 a=2b=1故化学方程式中a和b的比为2∶1是正确的,故选A

练习册系列答案
相关题目