题目内容
【题目】如图为A、B、C、D四种粒子的结构示意图以及硒元素在元素周期表中的信息,请按要求填空
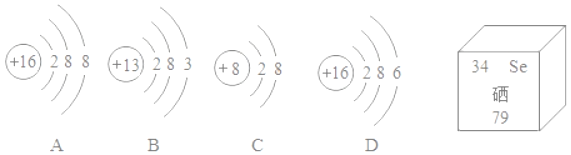
(1)A、B、C、D四种粒子中,属于同种元素的是_____(填序号)A粒子的符号为_____。
(2)由B元素和C元素形成的化合物的化学式为_____。
(3)该硒原子的中子数是_____。
(4)不同元素的原子中,下列各项肯定不相同的是_____。(填序号)
①中子数②质子数③电子层数④核外电子总数⑤最外层电子数⑥核电荷数
【答案】AD; S2﹣ Al2O3 45 ②④⑥
【解析】
(1)A、B、C、D四种粒子中,属于同种元素的是AD,这是因为它们的核内质子数相等;
A粒子是带2个单位负电荷的硫离子,可以表示为S2﹣;
(2)由B元素(铝元素)和C元素(氧元素)形成的化合物是氧化铝,氧化铝中铝元素的化合价是+3,氧元素的化合价是﹣2,根据化合物中元素化合价代数和为零可知,氧化铝中铝原子和氧原子的个数比是2:3,氧化铝可以表示为Al2O3;
(3)在原子中,由质子数=电子数=核电荷数=原子序数及相对原子质量=质子数+中子数可知,该硒原子的中子数是:79﹣34=45;
(4)不同元素的原子中,由于元素种类不同,则核电荷数、质子数和核外电子总数肯定不同,故选②④⑥。

【题目】化学课上,同学们将氢氧化钠溶液和稀硫酸混合,没有观察到明显的现象,他对此提出了如下问题并进行了相应探究。
问题一:二者之间是否发生了反应?他们设计了如下方案证明二者之间确实发生了反应。
(1)下列组合能够证明二者确实发生了反应的有______。(填序号)

编号 | 试剂A | 试剂B |
① | 足量稀硫酸 | MgCl2溶液 |
② | 足量稀硫酸 | 铁粉 |
③ | 少量稀硫酸 | MgCl2溶液 |
④ | 少量稀硫酸 | 铁粉 |
(2)小兰认为,若选用______,不管加入顺序如何,只需控制加入稀硫酸的量也能证明二者发生了反应
(3)该反应的化学方程式为______。
问题二:反应后溶液中溶质有哪些?
(猜想假设)猜想一:只有Na2SO4:猜想二:Na2SO4和______;猜想三:Na2SO4和H2SO4
(查阅资料)①Na2SO4溶液显中性,②Na2SO4+BaCl2=Ba2SO4↓+2NaCl
(实验操作)分别取少量反应后的溶液于试管中,进行如下实验:
实验编号 | 实验过程 | 实验现象 | 实验结论 |
① | 加入酚酞试液 | 不变红 | 猜想一成立 |
② | 加入少量BaCl2溶液 | 产生白色沉淀 | |
③ | 加入少量Na2CO3溶液 | ______ (填“有”或“无”)气泡产生 |
(实验反思)小娜认为,实验______(填实验编号)可省略。
小秋用精密仪器检测反应后溶液中离子的个数比,也得出了相同结论,则测得溶液中的Na+和SO42-个数比为______。