题目内容
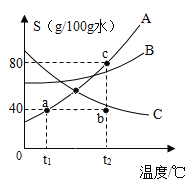
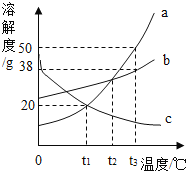
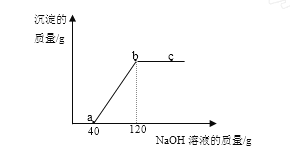
【题目】同学们向硫酸和硫酸铜的混合溶液中不断滴加溶质质量分数为10%的氢氧化钠溶液,加入的NaOH溶液与产生沉淀的质量关系,如图所示。
(1)加入氢氧化钠溶液一开始不产生沉淀的原因__________(写出反应的方程式),该反应________(填“是”或“不是”)中和反应。
(2)c点的pH__________7(填“>”、“<”或“=”),b点时溶液中所含溶质为____________(写化学式)。
(3)根据数据处理:求生成蓝色沉淀的质量(写出计算过程)__________。
【答案】 2NaOH+H2SO4 =Na2SO4+2H2O 是 > Na2SO4 9.8g
【解析】本题是图像与计算的综合题。由图像可知,向混合溶液中滴加氢氧化钠溶液先与硫酸反应,待混合溶液中硫酸完全反应后开始与硫酸铜溶液发生反应。在oa段发生氢氧化钠与硫酸反应,ab段则是氢氧化钠与硫酸铜的反应,达到b点时溶液中只含有硫酸钠, bc段则是向溶液中加入氢氧化钠但此时没有反应发生。
(1)向混合溶液中滴加氢氧化钠溶液先与硫酸反应,待混合溶液中硫酸完全反应后开始与硫酸铜溶液发生反应,加入氢氧化钠溶液一开始不产生沉淀的原因是氢氧化钠与硫酸反应生成硫酸钠和水,化学方程式是: 2NaOH+H2SO4 =Na2SO4+2H2O,该反应是酸和碱反应,生成盐和水,属于中和反应
(2)分析图像可知在oa段发生氢氧化钠与硫酸反应,ab段则是氢氧化钠与硫酸铜的反应,达到b点时恰好完全反应,溶液中只含有硫酸钠,化学式是Na2SO4, bc段则是向溶液中加入氢氧化钠但此时没有反应,c点时,氢氧化钠已过量,溶液呈碱性,pH>7;
(3)设:生成蓝色沉淀的质量为x,
ab段则是氢氧化钠与硫酸铜的反应,生成氢氧化铜的蓝色沉淀和硫酸钠,反应消耗的氢氧化钠的质量=(120g-40g)×10%=8g,
2NaOH+CuSO4═Na2SO4+Cu(OH)2↓
80 98
8g x
![]() x=9.8g。
x=9.8g。