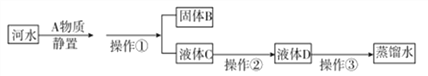
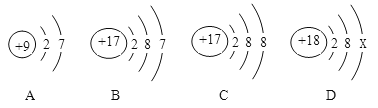题目内容
【题目】为测定某黄铜(铜、锌合金)中铜的质量分数,称取32.5g该黄铜粉末放入烧杯中,再向烧杯内加入200g稀硫酸(足量),每隔10分钟测烧杯内(不含烧杯)剩余物质的质量,测得数据如表:
加入稀硫酸后10分钟 | 加入稀硫酸后20分钟 | 加入稀硫酸后 | 加入稀硫酸后40分钟 | 加入稀硫酸后50分钟 |
232.4g | 232.3g | 232.2g | 232.1g | 232.1g |
(1)完全反应后生成氢气的质量为______g.
(2)计算该黄铜中铜的质量分数为________(写出计算过程).
【答案】 0.4 60%
【解析】解:(1)根据质量守恒定律可得,生成的氢气的质量为32.5g+200g﹣232.1g=0.4g
(2)设参加反应的锌的质量为x,
Zn+H2SO4=ZnSO4+H2↑
65 2
x 0.4g
![]()
x=13g
该黄铜中铜的质量分数为![]() ×100%=60%
×100%=60%
答:(1)完全反应后生成氢气的质量为0.4g;
(2)该黄铜中铜的质量分数为60%。

练习册系列答案
相关题目