题目内容
【题目】某市冬天取暖主要以煤为燃料。已知原煤中含硫1%,若燃烧1000 t这样的原煤可以产生二氧化硫________t,这些原煤中的硫元素全部转化成硫酸( S→H2SO4),可生产0.05%的硫酸溶液_________t,通过以上信息你得到哪些启示?(答出两点即可)________
【答案】 20 6.125×105 酸雨会给人类生活和生态带来严重危窖(如酸雨腐蚀大理石雕像、金属建筑物、破坏森林、酸化土壤等);使用脱硫煤;开发新能源代替现有的化石燃料等。
【解析】解:1000t原煤含硫:1000t×1%=10t
设10t硫可以产生二氧化硫x
S+O2 ![]() SO2
SO2
32 64
10t x
![]()
x=20t
设10t硫可生成硫酸y
2S+3O2+2H2O=2H2SO4
64 196
10t y
![]()
y=30.625t
设30.625t硫酸可产生0.005%的硫酸溶液Z
Z×0.005%=30.625t
Z= 612500t
根据以上数据可知,①酸雨会给人类生活和生态带来严重危害(如酸雨能腐蚀建筑物、毁坏树木、污染水体等);
②使用脱硫煤能防止酸雨的产生,开发新能源能防止环境污染等。

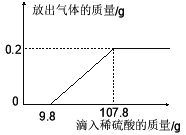
【题目】为测定某黄铜(铜、锌合金)中铜的质量分数,称取32.5g该黄铜粉末放入烧杯中,再向烧杯内加入200g稀硫酸(足量),每隔10分钟测烧杯内(不含烧杯)剩余物质的质量,测得数据如表:
加入稀硫酸后10分钟 | 加入稀硫酸后20分钟 | 加入稀硫酸后 | 加入稀硫酸后40分钟 | 加入稀硫酸后50分钟 |
232.4g | 232.3g | 232.2g | 232.1g | 232.1g |
(1)完全反应后生成氢气的质量为______g.
(2)计算该黄铜中铜的质量分数为________(写出计算过程).
【题目】一天,实验助手小娟走进实验室,和老师一起检查每个实验桌上的药品、仪器是否齐备,走到某组的时候,看到了一个不和谐的“音符”(如下图) .
(1)此情此景你首先想到的是它可能变质了,该变质反应的化学方程式为:_______________.
(2)围绕此瓶NaOH溶液是否变质的问题,小娟利用实验室的三种试剂(氯化钙溶液、稀盐酸、酚酞试液)展开了探究活动.
①取少量溶液于试管中,滴加某种试剂,有气泡产生,由此证明NaOH溶液已经变质.你认为小娟所加的试剂是_________________.
②欲证明变质的溶液中尚存NaOH,请你帮助小娟完成以下探究方案:
探究目的 | 探究步骤 | 预计现象 |
除尽溶液中的CO32- | ①取少量溶液于试管中,滴加足量的__________试剂 | 有白色沉淀产生 |
证明溶液中尚存NaOH | ②向实验①所得溶液中滴加酚酞试液 | __________________ |
(3)通过上述探究,说明氢氧化钠溶液暴露在空气中容易变质,故应__________保存.
【题目】实验课上,同学们利用如图所示装置进行气体制备。
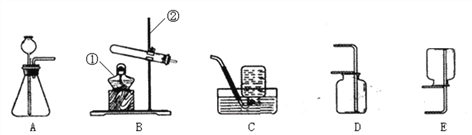
(1)写出图中有标号的仪器的名称:①___________、②__________。
(2)反应原理:实验室用加热高锰酸钾制取氧气的文字表达式为______________。用大理石和稀盐酸制取二氧化碳的文字表达式为____________________。
(3)气体制备:二氧化碳的发生装置是__________(填序号,下同)。
(4)气体的收集:实验室收集氧气的装置可选用___________,选择该收集方法是根据氧气具有_________________的性质。
(5)气体的检验:
气体 | 检验方法 | 实验现象 |
O2 | ______________ | ______________ |
CO2 | ______________ | ______________ |
(6)氨气(NH3)是一种密度比空气小,极易溶于水的气体,实验室可用加热氯化铵和氢氧化钙固体混合物制得氨气。氨气在加热条件下能与氧化铜反应生成铜、水和空气中含量最多的气体。制取氨气应选择_______和________装置连接。请写出氨气和氧化铜(CuO)反应的文字表达式_______________________________。