题目内容
【题目】实验与探究是化学学习的重要方法,请以碳及其化合物的知识探究以下问题。
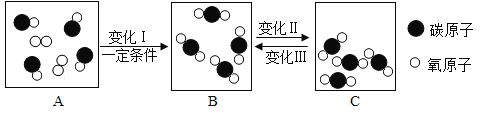
①探究一:木炭与氧化铜在一定条件下发生反应。甲同学查阅资料后,建议用超细炭粉与氧化铜粉末混合进行实验,他的理由是_______________。
②探究二:现有混有少量二氧化碳的一氧化碳气体,乙同学为了检验两种气体的存在,用如下装置进行实验。
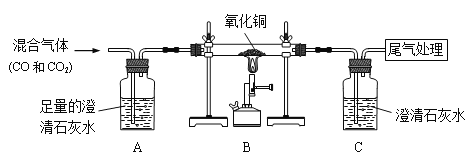
I.A装置的作用是_______________,产生的现象是__________________。
II.B装置中发生反应的化学方程式是______________,其中氧化铜发生_______(填“氧化”或“还原”)反应。
III.C装置中尾气处理的方法是______________(写出一种)。
③探究三:人们曾用贝壳(主要成分是碳酸钙,杂质不参加反应且不溶于水)和碳酸钠(俗名:纯碱)为原料制取氢氧化钠,丙同学按下图所示流程进行实验。
(提示:碳酸钠能与氢氧化钙反应,化学方程式为Na2CO3 + Ca(OH)2 → CaCO3↓ + 2NaOH)
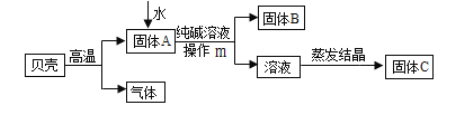
I.贝壳高温煅烧时,该反应的基本类型是________(填“化合”或“分解”)。
II.流程中操作m是_________;将溶液蒸发结晶至___________时停止加热。
III.将固体C配成溶液,其溶液中一定含有的溶质是________________。
【答案】增大反应物的接触面积,使反应更充分 检验和充分吸收混合气体中二氧化碳 澄清石灰水变浑浊 CO+ CuO高温 Cu+CO2 还原 气球收集或点燃(或在尾气出口处放一点燃的酒精灯) 分解 过滤 较多固体析出 氢氧化钠(NaOH)
【解析】
(1)物质的颗粒越小,物质间接触越充分,反应就越迅速、越彻底,所以用超细炭粉与氧化铜粉末混合进行实验,效果好;(2). 检验和充分吸收混合气体中二氧化碳 (3). 澄清石灰水变浑浊 (4).一氧化碳和氧化铜反应生成铜和二氧化碳,反应方程式为: CO+ CuO 高温 Cu+CO2 (5). 氧化铜发生的是失氧的反应,属于还原反应 (6). 一氧化碳是气体污染物,所以应将尾气进行处理,防止污染空气,措施是气球收集或点燃(或在尾气出口处放一点燃的酒精灯) (7). 碳酸钙在高温条件下生成氧化钙和二氧化碳, 由一种物质生成两种或两种以上物质的反应叫分解反应; (8). 过滤能将难溶性固体和液体分离 (9).蒸发操作时,要有较多固体析出(或少量液体剩余)时停止加热 (10). Na2CO3 + Ca(OH)2 =CaCO3↓ + 2NaOH ,所以过滤后的溶液中有氢氧化钠(NaOH),最终得到的固体纵也有氢氧化钠。

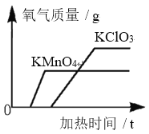
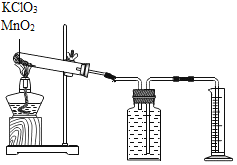
【题目】探究氯酸钾和二氧化锰制氧气实验中反应物与催化剂的最佳质量比。实验中采用如图实验装置,取20g氯酸钾,分成10等份,每份2g,分别装入10支试管中。在10支试管中分别加入不同质量的二氧化锰,分别测量二氧化锰与氯酸钾在不同质量比时,生成200mL氧气所消耗的时间。实验记录的数据如下:
实验编号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
二氧化锰质量(g) | 0.1 | 0.2 | 0.33 | 0.4 | 0.5 | 0.66 | 1 | 1.3 | 2 | 3 |
二氧化锰与氯酸钾的质量比 | 1:20 | 1:10 | 1:6 | 1:5 | 1:4 | 1:3 | 1:2 | 2:3 | 1:1 | 3:2 |
生成200mL氧气时间(秒) | 235 | 186 | 162 | 147 | 133 | 117 | 143 | 160 | 211 | 244 |
请回答下列问题:
(1)实验中收集一定体积的氧气采用的实验方法利用了氧气_____的性质。收集气体前集气瓶内未装满水,对实验结果_____(填“有”或“没有”)影响。
(2)分析上述数据,你认为利用此法制氧气时,二氧化锰与氯酸钾的最佳质量比为_____。
(3)利用双氧水和二氧化锰的混合物制氧气比加热氯酸钾和二氧化锰混合物制氧气更好。请写出前者的两个优点:①_____;②_____。
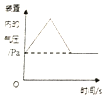
【题目】下列图象能正确反映对应变化关系的是( )
|
|
|
|
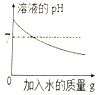
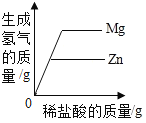
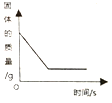
A.足量红磷在密闭容器中燃烧 | B.常温下,稀释KOH 溶液 | C.向等质量的Mg和Zn中分别加入等质量等浓度的稀盐酸 | D.将铁钉加入一定量的硫酸铜溶液中 |
A. A B. B C. C D. D
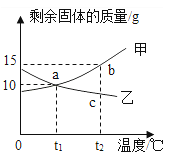
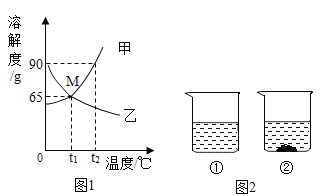
【题目】分析处理图表信息是学习化学的一种重要方法。下表是氯化钠和硝酸钾在不同温度下的溶解度,仔细阅读并回答下列问题。
温度/℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 70℃ | 80℃ |
氯化钠溶解度/g | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | 38.4 |
硝酸钾溶解度/g | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 |
(1)氯化钠和硝酸钾的溶解度随温度变化趋势更大的是_____(填化学式)。
(2)20℃时,将40g硝酸钾固体加入到100g水中,充分搅拌后静置,得到的溶液是硝酸钾的_____(填“饱和”或“不饱和”)溶液。若将温度升高到50℃,所得溶液溶质的质量分数为_____(精确到0.1%)。