题目内容
【题目】请根据下列装置图,回答有关问题:
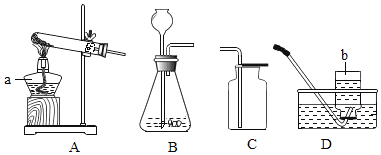
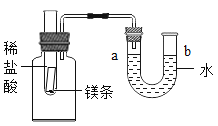
(1)写出装置图中标号仪器的名称:a_____,b_______。
(2)写出实验室用高锰酸钾制取氧气的化学方程式____,可选用的发生装置是____(填字母)。
(3)写出实验室用锌粒与稀硫酸制取氢气的化学方程式______,可选用的收集装置是_____(填字母)。
【答案】酒精灯 集气瓶 ![]() A
A ![]() D
D
【解析】
(1)仪器a为酒精灯;仪器b为集气瓶;
(2)高锰酸钾在加热的条件下反应生成锰酸钾、二氧化锰和氧气,该反应的化学方程式为:![]() ;
;
该反应属于固体加热反应,发生装置应选A;
(3)锌与稀硫酸反应生成硫酸锌和氢气,该反应的化学方程式为:![]() ;
;
氢气难溶于水,密度比空气小,可用排水法或向下排空气法收集,故收集装置应选D。

 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案【题目】Na2CO3在工业和生活中有重要的作用。它的来源主要有以下两种途径:
I.将制碱与制氨结合起来的联合制碱法。这个方法是由我国的制碱工业先驱_发明的。
A 张青莲
B 道尔顿
C 侯德榜
D 华罗庚
Ⅱ.自然界有很多咸水湖,人们通过“冬天捞喊,夏天晒盐”的方式获得湖盐,其中就含有Na2CO3。
(1)小明同学想对某夏天制得的湖盐样品成分进行探究,查阅资料后他对样品成分做出了三种猜想。
猜想一:NaCl、Na2CO3
猜想二:NaCl、Na2SO4;
猜想三:NaCl、Na2CO3、Na2SO4请帮助他完成如下实验:
实验操作 | 实验现象 | 实验结论 | |
实验一 | 取少量样品于试管中,加适量水溶解后,加入过量稀HNO3 | 产生能使澄清石灰水变浑浊的气体 | 猜想___不成立 |
实验二 | 向实验一所得的溶液中加入适量的________ | __ | 猜想三成立 |
(2)小明同学为进一步确定上述湖盐样品中Na2CO3 的质量分数,取该湖盐样品10.0g做了如图所示的补充实验。(注:所用药品均足量)
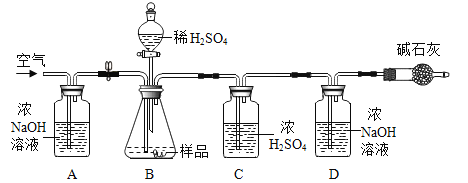
①反应结束之后打开止水夹并通入空气的目的是____。
②装置D中发生的反应为____(用化学方程式表示)。
③实验中碱石灰(含氧化钙和氢氧化钠)的作用是___。
④实验结束后,测得装置D增重0.33g,则该湖盐样品中Na2CO3的质量分数为多少___?