题目内容
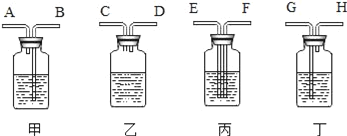
【题目】实验室常用以下装置制取气体,请根据要求回答问题。
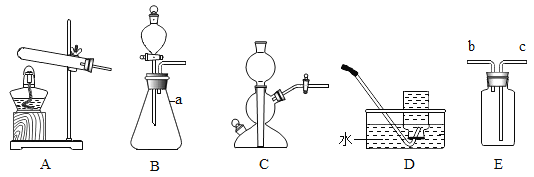
(1)写出仪器编号a的名称_______。
(2)实验室制取干燥氧气时,可以选用的装置是______(填装置编号),检验气体集满的方法是_______,反应的化学方程式是_______,反应基本类型是______。
(3)关于B与C装置相同点描述正确的是______。
I都可以随时添加液体
II装置上的活塞都能控制反应的发生与停止
III都可以控制反应的速率
IV都适用于固体与液体常温下的反应
(4)实验室用5%过氧化氢溶液和二氧化锰制取氧气,充分反应后得到0.05mol氧气,请问至少需要多少g过氧化氢溶液?(根据化学方程式列式计算)_______
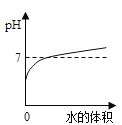
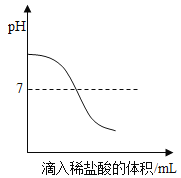
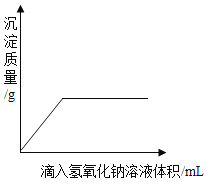
(5)小亮同学在实验室中制取CO2气体后,对废液进行后续探究,他向一定质量的含CaCl2和HCl的废液中逐滴加入溶质质量分数为10%的Na2CO3溶液。实验过程中加入Na2CO3溶液的质量与生成沉淀或气体的质量关系如图1所示,加入Na2CO3溶液的质量与溶液的pH变化关系如图2所示。

I 图1中0a段的现象是_______。图1中bc段涉及反应的化学方程式是_______。
II 图2中dh段之间(不包含d和h两点)溶液的溶质有______。
III 说法错误的是_______。
A图1中bc段反应过程中溶液的pH变化对应图2中hk段
B图1中a与b两点的溶液状态不同
C由图1和图2可推断CaCl2溶液显中性
D图1中x=2b
【答案】锥形瓶 AE 在b口放一带火星的木条,若木条复燃则氧气收集满  分解反应 I、IV 68克 产生气泡 Na2CO3+2CaCl2=CaCO3↓+2NaCl HCl、NaCl、CaCl2 B
分解反应 I、IV 68克 产生气泡 Na2CO3+2CaCl2=CaCO3↓+2NaCl HCl、NaCl、CaCl2 B
【解析】
(1)仪器a是锥形瓶,常用来做反应容器;故填:锥形瓶。
(2)实验室制取干燥的氧气可选用固固加热型发生装置,用排空气法进行收集,所以选择A和E两个装置,因为氧气的密度比空气大所以进行收集氧气时要长进短出,故E装置进行验满氧气的时候只需在b口放一带火星的木条,若木条复燃则阳气收集满,又因A装置中试管内没有棉花,所以选用的是氯酸钾制取氧气,反应的方程式为 ,该反应是一变多类型,属于分解反应。故填:AE;在b口放一带火星的木条,若木条复燃则氧气收集满;
,该反应是一变多类型,属于分解反应。故填:AE;在b口放一带火星的木条,若木条复燃则氧气收集满; ;分解反应。
;分解反应。
(3)B装置可通过分液漏斗上方随时添加液体,C装置可通过球形漏斗上方随时添加液体,故I正确;B装置中可以通过分液漏斗的活塞来控制液体滴加的速率从而控制反应速率,C装置是利用关闭旋塞,容器中压强增大,将液体压回球形漏斗,使容器中液体液面降低,与固体脱离接触,反应停止,因此B装置是能控制反应速率,而C装置是能控制反应的发生和停止,故II和III错误;装置B和装置C中都没有酒精灯,适合的是固液不加热型的反应,故IV正确;故填:I、IV。
(4)根据![]() ,可知0.05mol氧气的质量为1.6g。
,可知0.05mol氧气的质量为1.6g。
设:生成1.6g氧气需要过氧化氢的质量为x。
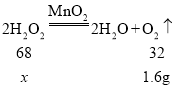
![]()
x=3.4g
所需过氧化氢溶液的质量=3.4g÷5%=68g
答:至少需要68g过氧化氢溶液。
(5)I、加入的碳酸钠先与盐酸反应,把盐酸消耗完了,才开始与氯化钙反应,开始生成沉淀,最后到达最高点说明已经反应完了,所以图1中0a段表示的是碳酸钠和盐酸反应生成气体的过程;bc段表示碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠的过程;故填:产生气泡;Na2CO3+2CaCl2=CaCO3↓+2NaCl。
II、图2中dh段溶液的酸性不断减少可知是碳酸钠和盐酸反应,hk段pH一直为中性是氯化钙和碳酸钠反应,即dh段氯化钙还没有开始反应,所以溶液中有氯化钙以及碳酸钠和盐酸反应生成的氯化钠和还没有反应完的盐酸。故填:HCl、NaCl、CaCl2。
III、A、图1中bc段是指的碳酸钠和氯化钙的反应,图2中hk段指的也是碳酸钠和氯化钙的反应,故A正确,不符合题意;
B、图1中a点代表的是盐酸的反应结束,图b点代表的是氯化钙反应的开始,溶液中的成分都是氯化钠和氯化钙,是一样的,故B错误,符合题意;
C、因为hk段的pH值一直为中性,所以可以由图1和图2推断出CaCl2溶液显中性,故C正确,不符合题意;
D、盐酸和碳酸钠反应生成2.2g二氧化碳需要5.3gNa2CO3,氯化钙和碳酸钠反应生成5g碳酸钙沉淀需要5.3gNa2CO3,x是指这两个反应中消耗的碳酸钠,所以x=2b,故D正确,不符合题意。
故选B。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案