题目内容
在实验课上,老师给了同学们一包红色的粉末,该粉末是铜粉和氧化铁中的一种或两种.同学们为了确定该粉末的成分,进行了如下探究。请你参与他们的探究并回答问题.
(1) [提出假设] 假设1:红色粉末是铜粉; 假设2:红色粉末是氧化铁粉;
假设3:红色粉末是 .
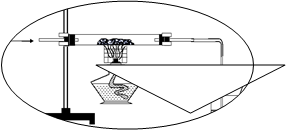
(2) [设计实验方案]同学们对实验作了如下的设想和分析:取少量红色的粉末放入硬质的玻璃管中,通入一氧化碳,加热至充分反应(如下图)。请你完成下列表格:
(3) 通过分析假设3成立.
(4) [反思与评价]
①实验时通入一氧化碳片刻后加热的原因是
.
②指出上述设计的实验中不足之处
.
③以氧化铁为原料,用上述方法炼铁的反应化学方程式______________________________

(1) [提出假设] 假设1:红色粉末是铜粉; 假设2:红色粉末是氧化铁粉;
假设3:红色粉末是 .
(2) [设计实验方案]同学们对实验作了如下的设想和分析:取少量红色的粉末放入硬质的玻璃管中,通入一氧化碳,加热至充分反应(如下图)。请你完成下列表格:
| 实验中可能出现的现象 | 结论 |
| | 假设1成立 |
| | 假设2成立 |
| | 假设3成立 |
(3) 通过分析假设3成立.
(4) [反思与评价]
①实验时通入一氧化碳片刻后加热的原因是
.
②指出上述设计的实验中不足之处
.
③以氧化铁为原料,用上述方法炼铁的反应化学方程式______________________________
铜粉和氧化铁粉
 (4)排尽装置内的空气,防止一氧化碳与空气混合加热发生爆炸
(4)排尽装置内的空气,防止一氧化碳与空气混合加热发生爆炸
没有进行尾气处理 Fe2O3+3CO===2Fe+3CO2
| 实验中可能出现的现象 | 结论 |
| 红色粉末不变色,澄清石灰水不变浑浊 | 假设1成立 |
| 红色粉末全部变黑色,澄清石灰水变浑浊 | 假设2成立 |
| 红色粉末部分变黑色,澄清石灰水变浑浊 | 假设3成立 |
 (4)排尽装置内的空气,防止一氧化碳与空气混合加热发生爆炸
(4)排尽装置内的空气,防止一氧化碳与空气混合加热发生爆炸没有进行尾气处理 Fe2O3+3CO===2Fe+3CO2
试题分析:(1)该粉末是铜粉和氧化铁粉中的一种或两种,因此红色粉末可能为两物质的混合物,
故答案为,铜粉和氧化铁粉的混合物,
(2)铜在高温下不与一氧化碳反应,因此粉末不变色,澄清石灰水也不会出现浑浊,氧化铁在高温下可与一氧化碳反应生成黑色铁粉和二氧化碳,充分反应后,粉末变黑色,澄清石灰水浑浊,故答案为:
| 实验中可能出现的现象 | 结论 |
| 红色粉末不变色,澄清石灰水不变浑浊 | 假设1成立 |
| 红色粉末全部变黑色,澄清石灰水变浑浊 | 假设2成立 |
| 红色粉末部分变黑色,澄清石灰水变浑浊 | 假设3成立 |
故答案为:Fe2O3+3CO===2Fe+3CO2,
②一氧化碳具有可燃性,与空气混合点燃可能发生爆炸,因此应先通一氧化碳,待玻璃管内气体为纯净的一氧化碳时再进行加热,防止形成混合气体而引起爆炸,
故答案为:防止加热一氧化碳和空气的混合气体时发生爆炸,
③一氧化碳气体有毒,直接排放到空气中会造成空气污染,可把尾气进行燃烧或收集,
故答案为:在b处用酒精灯点燃,或用塑料袋(气球)收集。
点评:解答此题的关键是了解在使用可燃性气体时,一定要注意检验气体的纯度,不纯的气体在点燃时有可能出现爆炸,可能气体主要有:氢气、一氧化碳、甲烷(天然气)。

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目



