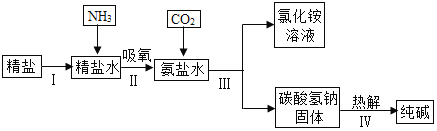
��Ŀ����
����Ŀ��ij��ȤС������֤���ᾧ�壨H2C2O4��2H2O�����ȷֽ������������̷�����̽���������£�
���������ϣ�
��1����֪���ᾧ�壨H2C2O4��2H2O����һ����ɫ���壬100�濪ʼʧˮ��101.5�����ҷֽ����H2O��CO��CO2����Ӧ����ʽΪ��H2C2O4��2H2O![]() CO��+ CO2��+3H2O��
CO��+ CO2��+3H2O��
��2��Ũ���������ˮ�ԣ�����������������
��3����ɫ����ˮ����ͭ��ˮ��������ɫ��
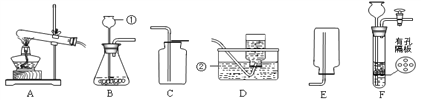
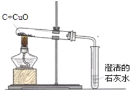
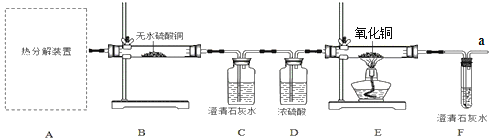
��ʵ����ƣ�����ͼ��ʾװ�ý���ʵ�飨װ��C��F�г���ʯ��ˮ������
���������ۣ�
��1�����п�����A�в��ᾧ���ȷֽ�װ�õ���________����ס����ҡ���������
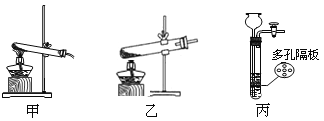
��2������ȤС���������ʵ��ʱ���ȵ�ȼ�ȷֽ�װ���еľƾ��ƣ�һ��ʱ����ٵ�ȼE���ľƾ��ƣ�ԭ����________��
��3��ʵ������й۲쵽��B�а�ɫ��ˮCuSO4�����ɫ��C��F�г���ʯ��ˮ������ǣ�E��____����ʵ���������֤���������������ȷֽ�����������H2O��CO2��CO ��E�з�Ӧ����ʽ��___��
��4����ͨ��Fװ���г���ʯ��ˮ�������֤�����ᾧ���ȷֽ�������������CO��������C��Dװ��֮������ʢ�г���ʯ��ˮ��ϴ��ƿ����������__________��
��5���ӻ����Ƕȿ��ǣ�����ʵ��װ��������ȱ�ݣ���Ľ���ʽΪ________��
������̽����
��6��������E�����ɵ�ͭ��ϡ���������������ּ��ȷ���һ��ʱ�����Һ��ʼ��ɵ���ɫ��ͬʱ�����϶�����ݣ����ɵ���ʲô�����أ�������ٿ�����H2 ���ڿ�����NO2 ���ۿ�����SO2 ��������Ϊ����_________������ţ�һ���Ǵ���ģ�������_______��
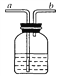
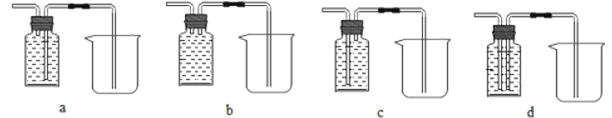
��7����С��ͬѧ��Ϊa����β���е�һ����̼�������ã����ǽ�a����������װ�����ӣ���ȥβ���еĶ�����̼���ռ�һ����̼�������к�����̽���������������װ����______�����a��b��c��d����ƿ��Ϊ����������Һ��������β���е�CO2����
������������
��8�������1.4��һ����̼��E������������ͭ��ȫ��Ӧ�����ɵ�������ȫ��F��������ʯ��ˮ������գ��ɵõ��������ٿ�______������д��������̣�
���𰸡��� ����װ���ڵĿ�������ֹ������һ����̼���ȱ�ը ��ɫ��ĩ��� CuO+CO![]() Cu+CO2 ֤��������̼�ѳ��� ��ȼ���ռ�β�� �� ��ѧ��Ӧǰ��Ԫ������� d 5��
Cu+CO2 ֤��������̼�ѳ��� ��ȼ���ռ�β�� �� ��ѧ��Ӧǰ��Ԫ������� d 5��
��������
��1����Ϊ��ʵ���Ŀ��������֤���ᾧ����ȷֽ������CO��CO2��H2O������װ��Ҫѡ���������ͣ���װ�ñ��ǹ�Һ�����ͣ�ѡ��װ������ʹ���ɵ�ˮ����˳���ӵ����ܵ�������2����ȼ����������������һ����ը���ޣ��ڱ�ը����Χ�ڣ��¶ȴﵽ�Ż��ᷢ����ը���˲�����Ŀ���Ǹ���װ���ڵĿ�������ֹ������һ����̼���ȱ�ը��
��3��E�з�Ӧ����ʽ��CuO+CO![]() Cu+CO2��CuO�Ǻ�ɫ���壬Cu�Ǻ�ɫ���壬����E��ʵ�������Ǻ�ɫ��ĩ�����
Cu+CO2��CuO�Ǻ�ɫ���壬Cu�Ǻ�ɫ���壬����E��ʵ�������Ǻ�ɫ��ĩ�����
��4������������ɵĶ�����̼���壬Fװ���г���ʯ��ˮ����ǣ�����֤������������һ����̼���塣��C��Dװ��֮������ʢ�г���ʯ��ˮ��ϴ��ƿ����������֤��������̼�ѳ�����
��5��β������һ����̼���壬Ӧ������һ��β������װ�á�
��6����ѧ��Ӧǰ��Ԫ�ص�����䣬��Ӧ������Ԫ�أ�����������NO2 ��
��7����ʵ��Ŀ������������ƿ��ȥ������̼���ռ�һ����̼��Ϊ��ʹ������̼������������Һ��ֽӴ���������˵ĵ�����Ӧ���dz��ģ�Ϊ�����ڽ�Һ���ų����Ҷ˵ĵ�����Ҳ�����dz��ģ���ѡd��
��8��CuO+CO![]() Cu+CO2��CO2 + Ca(OH)2 == CaCO3��+ H2O������CO-----------CaCO3����õ�������������x��
Cu+CO2��CO2 + Ca(OH)2 == CaCO3��+ H2O������CO-----------CaCO3����õ�������������x��
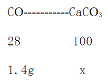
![]() =
=![]() �����x=5g
�����x=5g

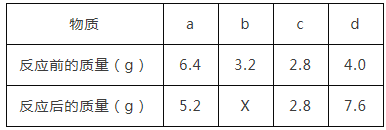
����Ŀ��ijͬѧΪ�˲ⶨʵ�������������Ʒ�Ĵ��ȡ�ȡ2.5�˸���Ʒ��0.5�˶������̻�ϣ�����һ��ʱ������ʲ��μӷ�Ӧ������ȴ������ʣ�����������ظ�������������¼�������±���
����ʱ�� | T1 | T2 | T3 | T4 |
ʣ�������� | 2.12 | 2.08 | 2.04 | 2.04 |
�ټ��ȵ�T2ʱ���������Ƿ��Ѿ���Ӧ��ȫ��_____
����Ʒ������ص���������_______