题目内容
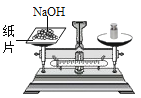
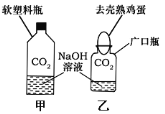
【题目】(1)U形管中是滴有酚酞溶液的蒸馏水,向左、右两管中同时逐滴滴加一定量的氢氧化钠稀溶液和稀盐酸(如图所示)。开始时_____管溶液呈红色。充分反应后U形管中溶液全部呈无色,除酚酞外,此时溶液中一定含有的溶质的名称为_____,可能含有的溶质的化学式为_____,

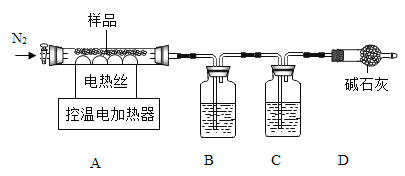
(2)氮气具有广泛用途,它是制造硝酸和氮肥的重要原料。写出含有氮元素的常用氧化物、酸、碱、盐的化学式各一个,并标出所写化学式中氮元素的化合价。氧化物_____、酸_____、碱_____、盐_____
(3)_____的雨水是酸雨。导致酸雨的空气污染物是_____。
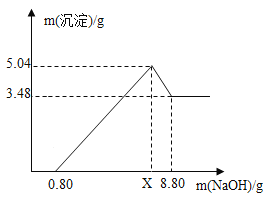
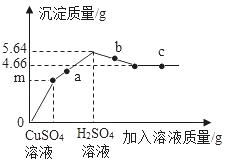
(4)某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图像,如图所示。
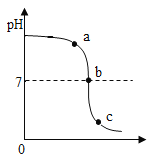
图中a点所示溶液中含有粒子有_____。从微观角度分析,该反应的实质是_____。
【答案】左 氯化钠 HCl ![]()
![]()
![]()
![]() pH<5.6 二氧化硫、氮氧化物等 钠离子、硫酸根离子、氢氧根离子、水分子 氢离子和氢氧根离子结合生成水分子
pH<5.6 二氧化硫、氮氧化物等 钠离子、硫酸根离子、氢氧根离子、水分子 氢离子和氢氧根离子结合生成水分子
【解析】
(1)氢氧化钠呈碱性,能使酚酞变红,稀盐酸呈酸性,使酚酞试液不变色,故开始时右边溶液为无色,左边溶液为红色;氢氧化钠与盐酸反应方程式为:NaOH+HCl═NaCl+H2O,充分反应后U形管溶液全部呈无色,可能显中性,也可能显酸性,因此除酚酞外,此时溶液中一定含有的溶质的名称为氯化钠,还可能含有氯化氢,其化学式为HCl;
(2)含有氮元素的常用氧化物、酸、碱、盐分别是一氧化氮、硝酸、氨水、硝酸钠,可分别表示为:![]() 、
、![]() 、
、![]() 、
、![]() ;
;
(3)pH<5.6的雨水为酸雨,导致酸雨的空气污染物是二氧化硫、氮氧化物等;
(4)a处的pH大于7,硫酸和氢氧化钠溶液反应生成硫酸钠和水,此时碱过量,则混合溶液中的溶质是硫酸钠和氢氧化钠,粒子有钠离子、硫酸根离子、氢氧根离子、水分子;从微观角度分析,该反应的实质是氢离子和氢氧根离子结合生成水分子。

 名校课堂系列答案
名校课堂系列答案【题目】KNO3和NaCl的溶解度表及溶解度曲线如下,下列说法错误的是
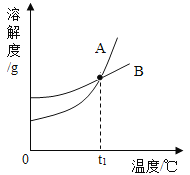
温度/℃ | 0 | 20 | 40 | 60 | 80 | |
溶解度 S/g | KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 |
NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | |
A.t1介于20℃-40℃之间
B.50℃时,溶液的溶质质量分数:KNO3>NaCl
C.当KNO3中混有少量NaCl时,可用蒸发结晶的方法提纯
D.60℃时,30g KNO3加入50g水,充分溶解,再降温到20℃,会析出晶体14.2g