题目内容
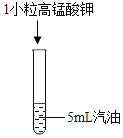
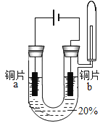
【题目】下列两个实验如图分别在试管中进行,回答问题。
①固体溶解 形成紫色溶液 |
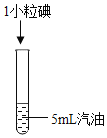
②固体几乎不溶解 |
③固体溶解, 形成紫红色溶液 |
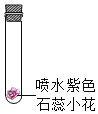
①紫色石蕊小花不变红 |
②紫色石蕊小花不变红 |
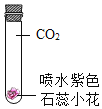
③紫色石蕊小花变红 |
A | B | ||||
(1)要想得出“碘在汽油中的溶解性比高锰酸钾好”,需要对比实验_____(填写序号即可)。
(2)对比B中实验①、②、③的现象,可得出的结论是_____。
【答案】A中实验②③ 二氧化碳和水反应生成了酸性物质
【解析】
二氧化碳和水反应生成碳酸。
(1)①、②对比,加入的物质相同,试管内的物质不同,则相同的溶质在不同的溶剂中溶解性不同;②、③中试管内均为5毫升的汽油,而加进去的物质不同,则实验的目的是探究不同的溶质在相同溶剂中的溶解性不同,故要想得出“碘在汽油中的溶解性比高锰酸钾 好”,需要对比A中实验②③。
(2)实验①中封口的试管内盛放的是二氧化碳和干燥紫色石蕊小花,实验目的是验证二氧化碳不能使干燥的紫色石蕊小花变色,实验①、②中的不同之处是②中无二氧化碳,小花被喷了水,证明了二氧化碳不能使干燥的石蕊变色,水也不能使石蕊变色,③中喷水的石蕊小花在有二氧化碳存在时变红,说明生成了新的物质,且新物质呈酸性,故对比B中实验①、②、③的现象,可得出的结论是二氧化碳和水反应生成酸性物质。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】在探究金属与酸的反应时,发现铜片与20%的硫酸溶液不反应。有同学提出疑问“在一定条件下铜与硫酸能否发生反应”,并进行了系列实验。
(查阅资料)SO2能让红色的品红溶液褪色,能被NaOH溶液吸收。
(进行实验)(夹持仪器略)
实验1:初步实验(所用溶液均为硫酸溶液)
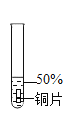
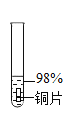
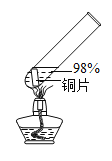
实验序号 | 1﹣1 | 1﹣2 | 1﹣3 | 1﹣4 | 1﹣5 |
装置 |
|
|
|
|
|
主要现象 | 铜片a附近溶液逐渐变蓝,铜片b附近产生无色气泡。 | 无明显现象 | 无明显现象 | 无明显现象 | 铜片溶解,溶液变蓝,生成有刺激性气味的无色气体 |
经检验实验1﹣1中产生的气体是氢气。
实验2:在实验1﹣5的基础上深入探究,装置如图。
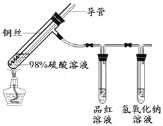
(解释与结论)
(1)实验1﹣1中,能证明铜发生反应的现象是_____。
(2)实验1中,欲得出“升高温度可使铜与硫酸反应”需对比的实验是_____(填实验序号)。
(3)补全实验1﹣5和实验2中铜与硫酸反应的化学方程式:![]() _____
_____
(4)与实验1﹣5相比,实验2的优点有_____(写出一条即可)。
(5)通过上述实验能得出的结论是_____。
(反思与评价)
(6)下列说法不正确的是_____。
A 对比实验1﹣2和1﹣5,可得出“增大浓度可使铜与硫酸反应”
B 通电可促进一些化学反应的发生
C 铜与硫酸只能发生一种化学反应
【题目】⑴化合物可以分为酸、碱、盐及氧化物。在下图中填写不同类别的物质__________(填化学式)实现Ca(OH)2一步转化为CaCO3。
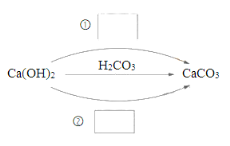
⑵某Ca(OH)2 样品部分变质为CaCO3 (假设其成分均匀)。化学兴趣小组按以下步骤测定该样品中Ca(OH)2 的质量分数。
①配制盐酸:配制500g质量分数为6%的盐酸,需要质量分数为30%的盐酸_____g。
②实验测定:
称取10.0g样品置于烧杯中,加入足量稀盐酸充分反应,烧杯总质量与反应时间的关系如下表所示:
反应时间/min | 0 | t1 | t2 | t3 |
烧杯总质量/g | 280.0 | 278.9 | 277.8 | 277.8 |
完全反应后,生成的CO2气体的质量为___________g。
③数据处理:计算该样品中Ca(OH)2 的质量分数________(根据化学方程式的计算写出完整的计算步骤)。