题目内容
【题目】写出下列反应的化学方程式。
(1)红磷在空气中燃烧______________。
(2)一氧化碳还原氧化铜______________。
(3)氢气的燃烧____________。
(4)过氧化氢溶液与二氧化锰混合制氧气_________________。
【答案】4P +5O2![]() 2P2O5 CO + CuO
2P2O5 CO + CuO![]() Cu+CO2 2H2+ O2
Cu+CO2 2H2+ O2![]() 2H2O 2H2O2
2H2O 2H2O2![]() 2H2O +O2↑
2H2O +O2↑
【解析】
(1)红磷在空气中燃烧生成五氧化二磷:4P +5O2![]() 2P2O5。
2P2O5。
(2)一氧化碳在加热条件下还原氧化铜生成铜和二氧化碳: CO + CuO![]() Cu+CO2。
Cu+CO2。
(3)氢气在氧气中燃烧生成水:2H2+ O2![]() 2H2O。
2H2O。
(4)过氧化氢溶液与二氧化锰混合生成水和氧气:2H2O2![]() 2H2O +O2↑。
2H2O +O2↑。

 名校课堂系列答案
名校课堂系列答案【题目】同学们在实验室用下图装置制取氧气。
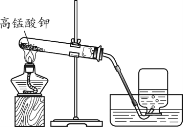
(1)加热高锰酸钾时,试管口略向下倾斜的原因是______。
实验后,同学们发现沾有高锰酸钾的白抹布洗完晾干后变为棕褐色。
(查阅资料)
草酸溶液能将棕褐色物质除去。
(提出问题)
哪些因素能加快草酸除去棕褐色物质的速率?
(进行实验)
将均匀染有棕褐色的抹布剪成大小相同的小布条进行实验
实验 编号 | 实验1
20℃ 水 | 实验2
20℃ 0.5%草酸溶液 | 实验3
20℃ 0.25%草酸溶液 | 实验4
20℃ 0.125%草酸溶液 | 实验5
30℃ 0.25%草酸溶液 | 实验6
40℃ 0.25%草酸溶液 |
现象 | 颜色 没有褪去 | 70秒后 颜色褪去 | 98秒后 颜色褪去 | 150秒后 颜色褪去 | 51秒后 颜色褪去 | 40秒后 颜色褪去 |
(解释与结论)
(2)配制200g溶质质量分数为 0.5%的草酸溶液,需要草酸的质量为______。
(3)实验1的目的是______。
(4)证明升高温度能加快草酸除去棕褐色物质的速率,需要对比______(填实验序号)。
(5)由实验2、3、4可以得出的结论是______。
(反思与评价)
(6)实验后,同学们查资料得知抹布上的棕褐色物质为二氧化锰,请你设计实验方案进行验证______。