题目内容
【题目】从微观视角认识和考察物质世界是学习化学的重要思维方法。
(1)下图是某反应的微观示意图:
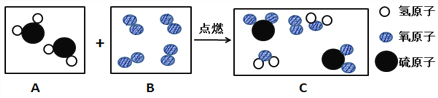
B框中的物质属于________(填序号:①化合物 ②单质 ③纯净物 ④混合物)。此反应化学方程式为____________________。
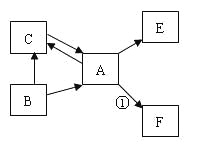
(2)写出下图A所示的反应化学方程式 _________________ ,属于_____________反应(填反应类型)。该反应前后,溶液减少的离子是 __________。下图B中反应溶液变为无色时,此时溶液中大量存在的粒子是_________________。

【答案】 ② 2H2S+3O2 ![]() 2SO2+2H2O 2KOH+H2SO4=K2SO4+2H2O 复分解 H+ 、OH - Zn2+ 、H2O、 SO42-
2SO2+2H2O 2KOH+H2SO4=K2SO4+2H2O 复分解 H+ 、OH - Zn2+ 、H2O、 SO42-
【解析】(1)B框中的物质为氧气,是同种原子构成的分子,属于单质,单质属于纯净物;根据分析,该反应是硫化氢和氧气点燃生成水和二氧化硫,去掉一个没有参加反应的氧气分子,微粒个数比为2:3:2:2,反应的化学方程式为:2H2S+3O2![]() 2SO2+2H2O;此图说明化学反应前后不发生改变的微粒是原子;(2)图A对比反应前后的微粒变化,反应前后钾离子和硫酸根离子没变说明该微粒实际没有参与反应,氢离子和氢氧根变了,反应后为水,故图A所示的反应化学方程式为2KOH+H2SO4=K2SO4+2H2O,属于复分解反应;该反应前后,溶液减少的离子是H+、OH。下图B中反应溶液变为无色时,此时溶液中存在的粒子是Zn2+、SO42、H2O。
2SO2+2H2O;此图说明化学反应前后不发生改变的微粒是原子;(2)图A对比反应前后的微粒变化,反应前后钾离子和硫酸根离子没变说明该微粒实际没有参与反应,氢离子和氢氧根变了,反应后为水,故图A所示的反应化学方程式为2KOH+H2SO4=K2SO4+2H2O,属于复分解反应;该反应前后,溶液减少的离子是H+、OH。下图B中反应溶液变为无色时,此时溶液中存在的粒子是Zn2+、SO42、H2O。

【题目】(1)我们已经学习了氢氧化钠的性质,知道这种固体要密封保存,原因有:①___________________;②________________。
兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验:
【对固体猜想】
猜想I:全部是NaOH;猜想II:全部是Na2CO3;猜想III:是NaOH和Na2CO3混合物
【实验和推断】
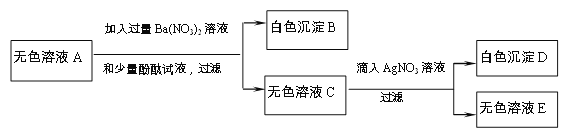
(2)为进一步确定成分,进行了以下探究:
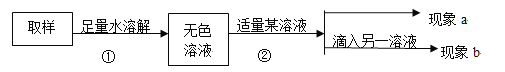
填写以下实验报告:
实验操作 | 实验现象 | 实验结论 |
第一步:用试管取约2mL该无色溶液,滴入适量澄清石灰水。 | 现象a:溶液变浑浊。 | 化学方程式:①___________, 证明有碳酸钠。 |
第二步:静置,取上层清液于另一试管中,滴入无色酚酞溶液。 | 现象b:②__________ | 证明含有NaOH,猜想III成立,是NaOH和Na2CO3混合物 |
③分析:小组中有同学提出质疑,认为以上实验不能证明猜想III成立,理由是:
a、Na2CO3溶液呈碱性; b、__________________________________________________。
(3)兴趣小组按下图实验测定部分变质的NaOH固体中Na2CO3的质量分数。
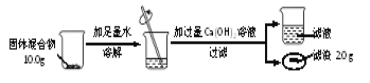
①根据题中信息______(填“能”或“不能”)计算Ca(OH)2溶液的质量分数。
②通过计算,固体混合物中Na2CO3的质量分数是__________________。