题目内容
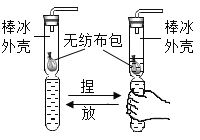
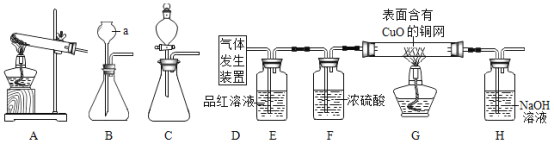
【题目】科学研究中常将不易观察、微观的现象或不易直接测量的通过实验的方法转换为易观察、宏观的现象或易测量的,此方法叫转换法。下列实验中,没有运用转换法的是( )
|
|
|
|
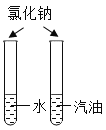
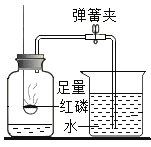
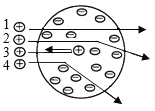
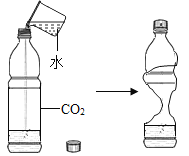
A.探究同种溶质在不同溶剂中的溶解性 | B.探究空气中氧气含量 | C.用a粒子轰击原子研究原子结构 | D.探究CO2的性质 |
A.AB.BC.CD.D
【答案】A
【解析】
A、氯化钠溶于水,不溶于汽油,可以通过观察实验直接探究氯化钠在水和汽油中的溶解性,不需要转换,符合题意;
B、因为氧气在空气中不可见,不易直接测量空气中氧气的含量,故使用转换法,将空气中的氧气完全消耗,再测量剩余的空气体积,即可知道氧气的体积,不符合题意;
C、因为原子非常小,不易直接研究原子结构,所以用a粒子轰击原子研究原子结构,不符合题意;
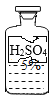
D、二氧化碳溶于水不易观察,故使用该装置,二氧化碳溶于水使瓶内气压减小,造成塑料水瓶的变形,不符合题意。故选A。

 天天向上口算本系列答案
天天向上口算本系列答案【题目】实验室常用加热氯酸钾和二氧化锰混合物的方法制取氧气,请回答下列问题:
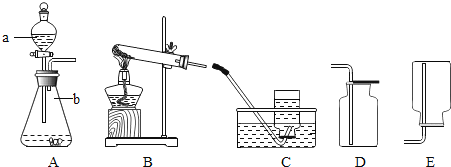
(1)反应的化学方程式为________.
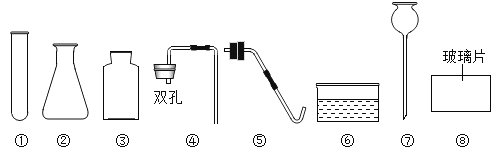
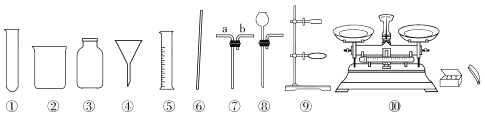
(2)写出下列编号仪器的名称![]() ________
________![]() ________.
________.
(3)用所给仪器组装用上述反应制氧气的装置,你选择的发生装置为________,![]() 装置试管口要略向下倾斜的原因是________;收集装置为________.
装置试管口要略向下倾斜的原因是________;收集装置为________.
上述装置选择的依据是________(填字母).
![]() 属于固固型加热的反应
属于固固型加热的反应 ![]() 属于固液型不加热的反应
属于固液型不加热的反应
![]() 制取的气体密度比空气大
制取的气体密度比空气大 ![]() 制取的气体难溶于水
制取的气体难溶于水
(4)若用图⑥装置进行“排空气法”收集制取的![]() ,请把图中的“导气管”补画完整_____.
,请把图中的“导气管”补画完整_____.
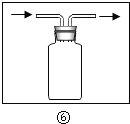
(5)有几位同学一起探究:氯酸钾和二氧化锰混合为多少比例时,产生氧气的速度最快.实验时用秒表记录时间,计时从加热到收集满一瓶氧气为准,实验所采用的装置是将![]() 和________组合起来.下表为二氧化锰与氯酸钾不同质量比时,制取氧气的速度比较
和________组合起来.下表为二氧化锰与氯酸钾不同质量比时,制取氧气的速度比较
实验序号 | 二氧化锰与氯酸钾的质量比 | 用时(秒) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
从实验序号![]() 和
和![]() 数据可以看出,实验序号________(填
数据可以看出,实验序号________(填![]() 或
或![]() )反应速度最快.通过分析可知,在化学反应中催化剂的用量(填“是”或“不是”)________越多越好.
)反应速度最快.通过分析可知,在化学反应中催化剂的用量(填“是”或“不是”)________越多越好.
(6)若在反应后的残余物中提纯![]() ,需进行以下操作,请把空缺处填上:_____、_____
,需进行以下操作,请把空缺处填上:_____、_____
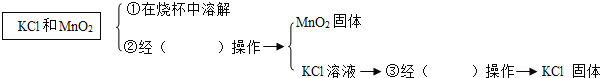
在①、②、③的操作中均用到的仪器是________.
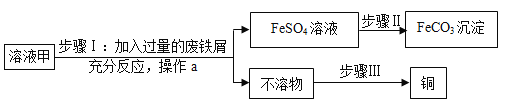
【题目】某化学兴趣小组的同学,通过咨询老师准备用亚硫酸钠溶液与浓硫酸反应来制备一定量的![]() ]。老师给他们提供了一瓶亚硫酸钠溶液并告知该瓶溶液放置时间可能较长,不知是否变质。兴趣小组的同学分成甲、乙两小组对该瓶亚硫酸钠溶液成分进行实验探究。
]。老师给他们提供了一瓶亚硫酸钠溶液并告知该瓶溶液放置时间可能较长,不知是否变质。兴趣小组的同学分成甲、乙两小组对该瓶亚硫酸钠溶液成分进行实验探究。
[提出问题]该瓶溶液中溶质的成分是什么?该瓶溶液中亚硫酸钠的质量分数是多少?
[查阅资料]
a、Na2SO3有较强还原性,在空气中易被氧气氧化:![]() ;
;
b、Na2SO3能与酸反应产生SO2气体;
c、SO32-、SO42-均能与Ba2+反应产生白色沉淀,BaSO3可溶于稀盐酸。
[作出猜想]
猜想1:没有变质,成分是Na2SO3;
猜想2:完全变质,成分是Na2SO4;
猜想3:部分变质,成分是Na2SO3和Na2SO4。
[实验探究I]甲组设计实验探究溶液是否变质:
甲组 | 实验操作 | 现象 | 结论 |
步骤1 | 取少量样品于试管中加入过量稀盐酸。 | 产生气泡 | 溶液中含有_____ |
步骤2 | _____ | _____ | 溶液中含有Na2SO4 |
实验结论是_____。
[实验探究Ⅱ]乙组设计如下实验测定Na2SO3溶液的溶质质量分数。
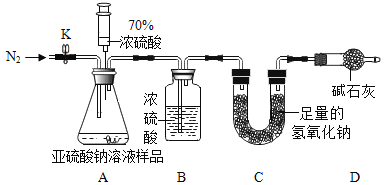
(1)连好装置并检查装置气密性,在锥形瓶中放人126g该样品,通入N2的目的是_____。
(2)实验前称量C装置的质量为128.8g。
(3)关闭活塞K,用注射器推入浓硫酸至不再产生气泡,注射器可以换为_____,也能控制液体试剂的滴加速率。
(4)打开活塞K,缓缓鼓入一定量的N2,继续通入N2的作用是_____。
(5)再次称量C装置的质量为135.2g。
(6)计算出该溶液中Na2SO3的质量分数为10%,若没有D装置,实验结果将_____(填“偏大”“不变”或“偏小”)。
[反思]由此可得出,保存亚硫酸钠时应_____。