题目内容
【题目】化学实验小组的同学在用锌粒与下图硫酸溶液(试剂瓶标签部分腐蚀)反应时,发现有气泡产生,并闻到有刺激性气味。他们对此气体的成分进行了探究。
[提出问题]锌粒加入该硫酸溶液反应生成的气体是什么?
[查阅资料]①浓硫酸与锌反应,但不产生氢气,也不会产生氧气,能生成二氧化硫气体;
②二氧化硫有刺激性气味,易溶于水,能使品红(一种红色色素)溶液褪色。
[猜想与假设]甲同学认为:气体可能是H2;
乙同学认为:气体可能是SO2;
丙同学认为:气体还可能是_____。
[实验探究]为了验证上述猜想,同学们在老师的指导下设计了如下图的装置(部分夹持器材略去,假设每个能发生的反应都进行完全)进行探究:
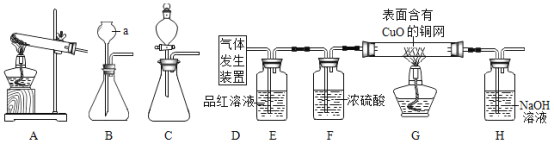
(1)图2中D处气体发生装置可选图1中的_____(填字母序号)。
(2)实验开始后,观察到E中品红溶液褪色,证明气体中含有_____。
(3)写出H装置中发生反应的化学方程式_____。
(4)G装置在点燃酒精灯加热之前应先通段时间的气体。目的是_____加热段时间后,观察到_____,证明气体中含有H2。
[实验结论]_____同学的猜想是正确的。
[反思与交流]
①锌和浓硫酸反应生成硫酸锌、水和二氧化硫,为什么反应过程中又产生了氢气呢?用文字简述原因:_____。
②锌与浓硫酸、稀硫酸反应都可以产生硫酸锌,如果需要制取硫酸锌,用锌与稀硫酸反应的优点是_____(任填一种合理的答案)。
【答案】H2和SO2 B或C SO2 ![]() 排尽装置内的空气 黑色固体变红 丙 随着反应的进行浓硫酸变成了稀硫酸 只产生氢气或无污染
排尽装置内的空气 黑色固体变红 丙 随着反应的进行浓硫酸变成了稀硫酸 只产生氢气或无污染
【解析】
锌和浓硫酸反应生成硫酸锌、氢气和二氧化硫,锌和稀硫酸反应生成硫酸锌和氢气,二氧化硫和氢氧化钠生成亚硫酸钠和水。
[猜想与假设]甲同学认为:气体可能是H2;
乙同学认为:气体可能是SO2;
丙同学认为:气体还可能是H2和SO2。
[实验探究]
(1)锌和稀硫酸反应生成硫酸锌和氢气,反应在常温下进行,选用固液常温型装置,故图2中D处气体发生装置可选图1中的B或C。
(2)二氧化硫有刺激性气味,易溶于水,能使品红(一种红色色素)溶液褪色,故实验开始后,观察到E中品红溶液褪色,证明气体中含有SO2。
(3)H装置中发生反应是二氧化硫和氢氧化钠生成亚硫酸钠和水,反应的化学方程式为![]() 。
。
(4)氢气是可燃性气体,不纯加热会发生爆炸,则G装置在点燃酒精灯加热之前应先通段时间的气体,目的是排尽装置内的空气,氢气和氧化铜加热生成铜和水,故加热段时间后,观察到黑色固体变红,证明气体中含有H2。
[实验结论] E装置中品红溶液褪色,说明生成二氧化硫,G装置中黑色固体变红,说明生成氢气,故丙同学的猜想是正确的。
[反思与交流]
①浓硫酸随着反应的进行变成稀硫酸,故锌和浓硫酸反应生成硫酸锌、水和二氧化硫,产生了氢气的原因是随着反应的进行浓硫酸变成了稀硫酸。
②锌与浓硫酸反应生成二氧化硫,二氧化硫有毒,污染空气,锌和稀硫酸反应生成氢气,无毒,故需要制取硫酸锌,用锌与稀硫酸反应的优点是只产生氢气或无污染。

 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案【题目】科学研究中常将不易观察、微观的现象或不易直接测量的通过实验的方法转换为易观察、宏观的现象或易测量的,此方法叫转换法。下列实验中,没有运用转换法的是( )
|
|
|
|
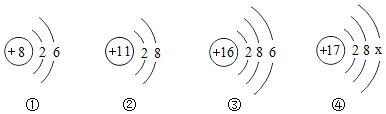
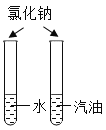
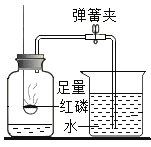
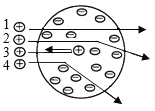
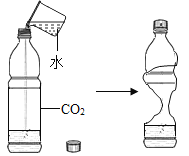
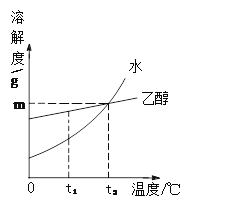
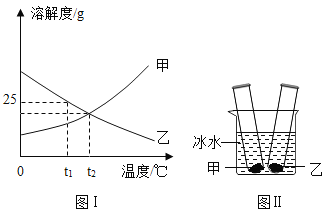
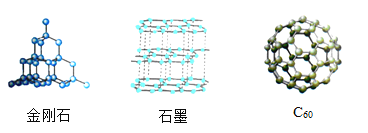
A.探究同种溶质在不同溶剂中的溶解性 | B.探究空气中氧气含量 | C.用a粒子轰击原子研究原子结构 | D.探究CO2的性质 |
A.AB.BC.CD.D