题目内容
用氢氧化钠溶液测定某硫酸溶液溶质的质量分数.实验如下:取25g该硫酸溶液,加入到烧杯中,然后把50g质量分数为10%的氢氧化钠溶液不断滴入烧杯中,同时用电子PH计不断读取反应时的PH,得出如图所示的关系,求;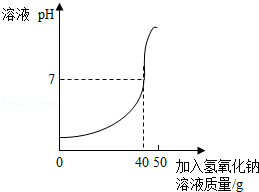
(1)该硫酸溶液溶质的质量分数.
(2)配制500g上述硫酸溶液,所需质量分数为98%的硫酸溶液的质量.
(1)19.6% (2)100g
解析试题分析:(1)当溶液的pH值等于7说明硫酸恰好和氢氧化钠溶液反应,此时消耗10%的氢氧化钠溶液40g.
设该硫酸溶液溶质的质量分数为x.
2NaOH+H2SO4=Na2SO4+2H2O
80 98
40g×10% 25g×x
x=19.6%
答:该硫酸溶液溶质的质量分数为19.6%.
(2)设所需质量分数为98%的硫酸溶液的质量为y.
500g×19.6%=y×98%
y=100g
答:所需质量分数为98%的硫酸溶液的质量为100g.
考点:根据化学反应方程式的计算;有关溶质质量分数的简单计算.
点评:本题是有关化学方程式和溶质质量分数的简单计算.解题时要注意格式和步骤.

长期使用的水壶底部都结有一层水垢,其主要成分是碳酸钙和氢氧化镁。为较准确测定水垢中氢氧化镁的含量,实验小组分别取三份同样的水垢样品各7.00g,利用如图所示装置连续进行三次实验,并将每次实验中装置B的质量变化记录于下表: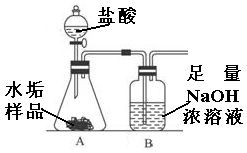
| | 第一次 | 第二次 | 第三次 | 平均值 |
| B装置增加的质量(g) | 2.17 | 2.22 | 2.21 | |
分析上面实验与数据后,回答:
⑴第一次实验测得数据较低的原因是 ;
⑵平均每份水垢样品中碳酸钙的质量为 克;
⑶水垢样品中氢氧化镁的平均质量分数为 。(计算结果精确到0.1)
某化工厂生产的纯碱中含有少量NaCl杂质,其产品包装袋上标有:碳酸钠≥96%.为了证实该产品中碳酸钠的含量,某同学取12g该样品放入烧杯中,称得烧杯和样品总质量为132.0g再把100g稀盐酸平均分成4次加入烧杯中,每次充分反应后烧杯和剩余物总质量如下:(每次反应产生的CO2气体都全部从烧杯中逸出)
| 加入稀盐酸次数 | 1 | 2 | 3 | 4 |
| 加入稀盐酸质量/g | 25 | 25 | 25 | 25 |
| 充分反应后烧杯和剩余物总质量/g | 155.2 | 178.4 | 202.6 | 227.6 |
请你根据表中数据分析:①第1次充分反应后产生的CO2气体质量是 g
②该产品中碳酸钠的质量分数是多少?该产品是否合格?(计算后回答,计算结果精确到0.1%)
将干燥管浸没烧杯或从烧杯中取出能达到随开随用随关随停。下列气体的制取可使用该装置的是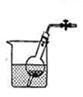
| A.用大理石粉末与稀盐酸反应制取二氧化碳 |
| B.用锌粒与稀硫酸反应制取氢气 |
| C.用二氧化锰粉末与双氧水溶液制氧气 |
| D.用块状大理石与稀盐酸反应制取二氧化碳 |
氯气有毒,实验室制取氯气的原理是:
MnO2+4HCl(浓)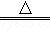 MnCl2+Cl2↑+2X.下列说法错误的是( )
MnCl2+Cl2↑+2X.下列说法错误的是( )
| A.可采用制取二氧化碳的装置制取氯气 |
| B.锰的化合价由+4降为+2 |
| C.收集时要有尾气处理装置 |
| D.X的化学是为H2O |
