题目内容
【题目】右图A、B、C三种固体物质的溶解度曲线。
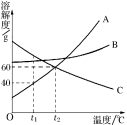
(1)t1℃时,A物质的饱和溶液中溶质的质量分数是 。
(2)使t1℃时C物质的不饱和溶液都变成饱和溶液,采用的方法是 (写一条)。
(3)t2℃时,B物质的溶解度 C物质的溶解度(填“大于”、“小于”或“等于”)。
【答案】(1)28.6%(2)升温或减少溶剂或增加溶质(3)大于
【解析】
试题分析:从图示看t1℃时,A的溶解度是40克,所以t1℃时,A物质的饱和溶液中溶质的质量分数是=40克/140克×100%=28.6%;使t1℃时C物质的不饱和溶液都变成饱和溶液,采用的方法是升温,因为C的溶解度随温度的升高而变小,减少溶剂或增加溶质也可以实现转变。t2℃时,B物质的溶解度大于C物质的溶解度。

【题目】研究和控制化学反应条件有重要意义。
(1)同学们想探究双氧水的浓度对反应速率的影响。在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间。
实验 | 双氧水的质量(g) | 双氧水浓度(%) | 二氧化锰质量(g) | 收集时间(s) |
1 | 50 | 6 | 5 | 200 |
2 | 50 | 12 | 5 | 100 |
3 | 50 | 18 | ______ | 67 |
①写出上述反应的文字表达式________________________。
②实验3中,加入的二氧化锰质量为___________g。
③相同条件下,实验3产生氧气的速率最快,说明________________________。
④同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气。
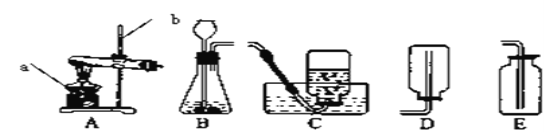
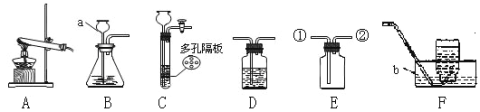
为了验证加热双氧水也可以产生氧气,同学们选择右图装置(气密性良好)进行实验。实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是________________,同学分析原因后,采用了____________法收集气体,再检验,证明加热双氧水也可产生氧气。
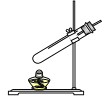
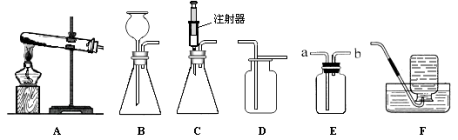
【题目】请结合下列实验常用装置,回答有关问题.
(一)(1)若用B、F组成制取某气体的装置,写出制取此气体的化学方程式为 ,若要获得干燥的二氧化碳,除发生装置外,还应选用D装置,并在该装置中盛放 试剂(填写试剂名称).如果用E装置收集该气体则气体从 端进入(填“①”或“②”)。
(2)乙炔(C2H2)是无色、无味、易燃的气体,乙炔的密度比空气略小,难溶于水。乙炔(C2H2)气体和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割或焊接金属。乙炔由碳化钙(块状固体)与水反应生成,同时生成一种白色固体。已知碳化钙与水反应非常剧烈。实验室欲制取并收集纯净的乙炔,要求做到节约、安全、随时发生、随时停止,你选择的装置是 。
(二)实验室里有一瓶常用的无色溶液,因保管不当,其残缺的标签中只剩下“Na”和“10%”字样(如图所示).
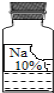
小强和小华同学很感兴趣,决定对其成分进行探究.
【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,这瓶试剂不可能是
A.酸 B.碱 C.盐
【查阅资料】
Ⅰ初中常见含钠的化合物有:NaCl、NaOH、Na2CO3、NaHCO3.
ⅡNa2CO3和NaHCO3的水溶液都呈碱性.
Ⅲ室温(20℃)时,测定四种物质的溶解度数据如下:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
溶解度g | 36 | 109 | 215 | 9.6 |
小华根据试剂瓶标注的质量分数为10%和上表中的溶解度数据判断,这瓶试剂不可能是
【作出猜想】①可能是NaCl;②可能是Na2CO3;③可能是
【实验探究】
(1)小强用洁净的玻璃棒蘸取试液于pH试纸上,测得pH>7,则这瓶试剂不可能是
(2)小强为了检验该溶液是NaOH溶液还是Na2CO3溶液,他又进行了如下实验.
实验步骤 | 实验现象 | 结论及化学方程式 |
取少量溶液于试管中,滴加 | 产生大量气泡 | 反应的化学方程式: |
② 把产生的气体通入澄清的石灰水中. | 澄清的石灰水变浑浊 | 猜想②正确. 反应的化学方程式: |