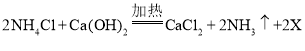题目内容
【题目】根据元素周期表中1﹣18号元素的排列情况。我对它进行探究:
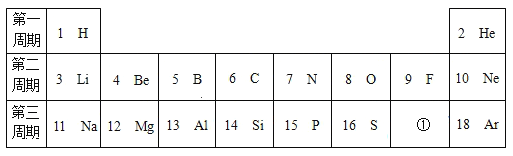
(1)第16号元素属于_____元素(填“金属”或“非金属”)。
(2)①表示的元素对应单质的化学式是_____。
(3)研究表明:在同一周期中,从左到右,原子失去电子的能力逐渐减弱,得到电子的能力逐渐增强。由此推断:第二周期中得电子能力最强的是_____(填名称)原子;第9号和第12号元素形成的化合物化学式是_____。
【答案】非金属 Cl2 氟 MgF2
【解析】
(1)第16号元素是硫元素,属于非金属元素;
(2)①表示的元素是氯元素,对应单质的化学式是Cl2;
(3)因为从同周期中从左到右,原子失去电子的能力逐渐减弱,得到电子的能力逐渐增强,所以第二周期中得电子能力最强的是9号元素F,第9和第12号元素分别为镁元素、氟元素,其化合价分别为+2、-1价,故形成化合物的化学式为MgF2。

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
【题目】为测定某氧化铜和铜的固体混合物中氧化铜的质量分数,小勇同学取20g固体混合物置于烧杯中,将100g稀硫酸分为四等份依次加入其中进行实验,测得数据如下:
次序 | ① | ② | ③ | ④ |
加入稀硫酸的质量/g | 25 | 25 | 25 | 25 |
剩余固体的质量/g | 16 | a | 10 | 10 |
回答列问题:
(1)原固体混合物中,氧化铜的质量分数为_____。
(2)上表中,a的值为_____,实验③所得溶液中的溶质是_____(填化学式)。
(3)该实验所用稀硫酸中溶质的质量分数为____。(写出计算过程,结果精确到0.1%)