题目内容
【题目】向含有碳酸钠和氢氧化钠的混合物溶液中逐滴加稀盐酸,充分反应后,产生气体的体积与加入稀盐酸的体积关系如图所示,请根据图像回答下列问题:
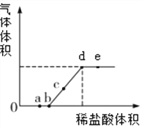
(1)ob段发生反应的基本类型是____________。
(2)bd段反应的化学方程式为____________。
(3)a、b、c、d、e五点对应的溶液中,含有两种溶质的有______________。
A.a B.b C.c D. d E.e
【答案】 复分解反应 Na2CO3 + 2HCl == 2NaCl+ H2O + CO2 ↑ BCE
【解析】由题目的信息可知:一定质量的NaOH溶液与Na2CO3溶液中逐滴加稀盐酸,稀盐酸优先于氢氧化钠反应,图中0b段表示的是氢氧化钡和盐酸反应生成氯化钠的过程,酸碱中和反应属于复分解反应;(2)bd段表示的是碳酸钠和盐酸反应生成气体的过程,化学方程式为:Na2CO3 + 2HCl == 2NaCl+ H2O + CO2↑;(3)a、b、c、d、e五点对应的溶液中,含有两种溶质的有:a表示氢氧化钠和盐酸反应生成氯化钠和水,此时溶质为碳酸钠、氯化钠和氯化氢;b点表示氢氧化钠和稀盐酸恰好完全反应生成氯化钠和水,此时溶质为氯化钠和碳酸钠;c表示碳酸钠与盐酸反应生成氯化钠、水二氧化碳,但碳酸钠有剩余,溶质为氯化钠和碳酸钠;d表示碳酸钠和盐酸完全反应,此时溶液中溶质为氯化钠;e表示盐酸过量,故溶液中溶质为氯化钠和氯化氢。故选BCE。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目