题目内容
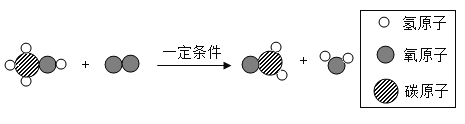
【题目】科学家发现,通过简单的化学反应可以制得甲烷,下图是该反应的微观示意图:

(1)该反应的基本反应类型是________;参加反应的A、B两物质的粒子个数比是________。
(2)由上图可获得的信息有___________(写一条)。
(3)写出甲烷燃烧的化学方程式:____________。
【答案】置换反应 3:4 化学反应中,分子可分成原子,原子不再分 CH4+2O2![]() CO2+2H2O
CO2+2H2O
【解析】
(1)由图可知,该反应是碳和氨气在催化剂和高温的条件下反应生成氮气和甲烷,反应的化学方程式写为:3C+4NH3 2N2+3CH4,该反应是一种单质与一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应,故填置换反应;
2N2+3CH4,该反应是一种单质与一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应,故填置换反应;
由化学方程式可做,参加反应的A(碳)、B(氨气)两物质的粒子个数比是3:4,故填3:4。
(2)由图可知,化学反应中,分子可分成原子,原子不再分,故填化学反应中,分子可分成原子,原子不再分。
(3)甲烷与氧气在点燃的条件下反应生成二氧化碳和水,故反应的化学方程式写为:CH4+2O2![]() CO2+2H2O。
CO2+2H2O。
。

 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案【题目】氢氧化钠是常见的碱,为探究氢氧化钠的化学性质,同学们做了如下实验:
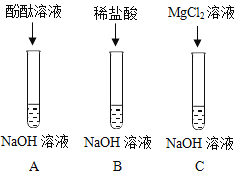
(资料)氯化镁溶液不能使酚酞溶液变红。
(1)A中溶液呈红色,说明氢氧化钠溶液显碱性,要测定它的酸碱度,可使用_____。
(2)B中没有明显的现象,该反应真的发生了吗?有同学提出,可向反应后的溶液中加入某些物质,根据相应的现象来判断,下列分析正确的有_____(填数字序号)
①加入Na2CO3溶液,如果不产生气泡,能证明反应发生
②加入CuSO4溶液,如果不产生蓝色沉淀,能证明反应发生。
③加入紫色石蕊溶液,如果溶液呈紫色,能证明反应发生。
(3)C中发生反应的化学方程式是_____。该实验证明碱能与某些盐反应。
(4)实验结束后,将三支试管中的物质倒入一只洁净的烧杯中,烧杯中出现白色沉淀,静置,上层清液无色。
(提出问题)上层清液中溶质的成分是什么呢?(指示剂除外)
(作出猜想)经过讨论,大家作出两种合理的猜想:
①NaCl;②______
(实验验证)将猜想②补充完整并设计实验加以验证。
实验操作 | 实验现象 | 结论 |
取少量上层清液于试管中,滴加____溶液 | _________ | 猜想②正确 |
老师提醒同学们,实验结束后氢氧化钠溶液仍要密封保存,原因是_____(用化学方程式表示)
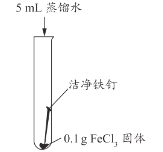
【题目】兴趣小组用稀盐酸除去铁钉表面的铁锈(主要成分是Fe2O3),发现反应开始时铁锈消失,有气泡产生,溶液颜色为黄色,一段时间后变为浅绿色。
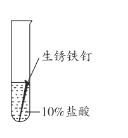
(查阅资料)FeCl3的溶液呈黄色
甲同学认为生成的FeCl3可能与试管中的物质继续反应,进行了下列实验。
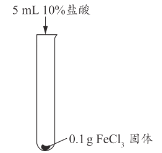
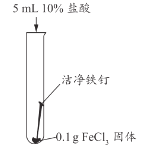
实验编号 | 实验1-1 | 实验1-2 | 实验1-3 |
实验操作 |
|
|
|
实验现象 | 长时间放置,溶液颜色始终为黄色 | 长时间放置,溶液逐渐从黄色变浅绿色 | 长时间放置,产生红褐色沉淀 |
(1)用盐酸除铁锈的化学方程式为_________。
(2)实验1-1的目的是_________。
(3)综合分析实验1,溶液从黄色变浅绿色的可能原因是_________。
乙同学用生锈程度相同的锈铁钉、5mL盐酸探究溶液颜色变化的影响因素。
实验编号 | 所用试剂 | 实验现象 | |
反应开始时 | 24h后 | ||
2-1 | 铁锈和2%盐酸 | 铁锈、溶液均无明显变化 | 铁锈消失,溶液变黄色 |
2-2 | 生锈铁钉和2%盐酸 | 生锈铁钉、溶液均无明显变化 | 铁锈消失,溶液变浅绿色 |
23 | 生锈铁钉和6%盐酸 | 铁钉表面有少量气泡,铁锈逐渐消失,溶液逐渐由无色变浅黄色 | 溶液变为浅绿色 |
2-4 | 生锈铁钉和10%盐酸 | 铁钉表面产生大量气泡,铁锈逐渐消失,溶液很快由无色变黄色 | 溶液变为浅绿色 |
(4)生锈铁钉与盐酸反应时,溶液的颜色变化与________有关。
(5)2-2中始终未观察到溶液变黄色,结合实验1和实验2推测可能的原因为______。
(6)基于上述实验推测,下列关于工业用盐酸除铁锈的说法合理的是______(填字母 序号)。
A 除铁锈时,所用盐酸的浓度越大越好
B 在除锈过程中,生成的FeCl3对铁也有腐蚀作用
C 用盐酸除锈时,应注意控制反应的时间
【题目】图一、图二是某兴趣小组探究金属、酸的化学性质时所做的两组实验。实验结束后,将两组实验试管中的物质分别全部倒入甲、乙两个洁净的烧杯中,据图回答:
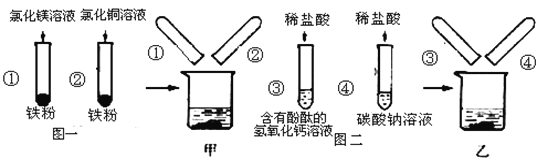
(1)在图一所示的实验中,试管②中发生反应的化学方程式是___________。
(2)将①②两只试管反应后的液体倒入甲烧杯中,发现红色固体物质明显增多。完全反应后,甲烧杯中的溶液中一定含有的阳离子是:_____________。
(3)当观察到③试管中的液体____________时,证明盐酸和氢氧化钙溶液能发生反应。
(4)将③④两只试管反应后的液体倒入乙烧杯中,观察到先有气泡产生,后有白色沉淀出现,溶液呈无色。则试管④反应后的溶液中的溶质共有哪些___________________(写化学式)。
(5)将乙烧杯内的物质进行过滤,对所得无色滤液中溶质成分进行了如下探究:
甲同学认为无色滤液中一定含有NaCl和 HCl,你认为甲同学的观点是否正确_________,其原因是:_________。
乙同学认为无色滤液中一定含有NaCl,一定不含有Na2CO3;
丙同学认为无色滤液中一定含有NaCl,还可能含有另外一种物质,于是做了如下实验:
实验操作 | 实验现象 | 实验结论 |
步骤1:取少量滤液于试管中,向其中滴加足量的__________溶液 | 有白色沉淀生成 | 滤液中的溶质有NaCl 和________ (写化学式) |