题目内容
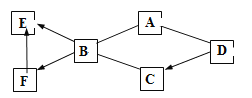
【题目】下列是镁元素、氯元素在元素周期表中的信息及有关粒子的结构示意图,请回答:
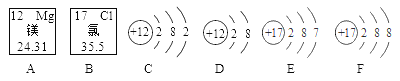
(1)D所表示的粒子是______(填化学符号),氯原子的结构示意图是_____(填序号);
(2)D、F形成的化合物的化学式是_______________;
(3)与元素的化学性质关系最密切的是_________(填序号)
①原子的核外电子数 ②元素的相对原子质量 ③原子的最外层电子数
【答案】 Mg2+ E MgCl2 ③
【解析】(1)根据圆圈内的数字及核外电子数分析解答;根据原子序数=质子数=核外电子数=17解答;(2)根据D是镁离子,F是氯离子分析解答;(3)根据原子的最外层电子数与元素的化学性质关系最密切解答。(1)D中圆圈内的数字是12,即为第12号元素----镁元素,又核外电子数为10,故D所表示的粒子是镁离子,符号为Mg2+;根据原子序数=质子数=核外电子数=17可知,氯原子的结构示意图是E;(2)D是镁离子,在形成化合物时通常显+2价,F是氯离子,在形成化合物时,通常显-1价,故D、F形成的化合物的化学式是MgCl2;(3)原子的最外层电子数与元素的化学性质关系最密切,故选③。

 名校课堂系列答案
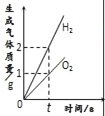
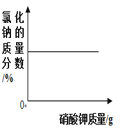
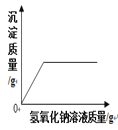
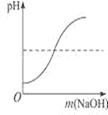
名校课堂系列答案【题目】下列图像能正确反映对应变化关系的是
|
|
|
|
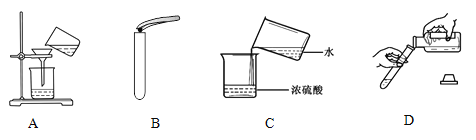
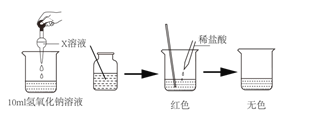
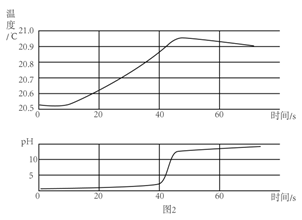
A.电解水产生氢气与氧气 | B.向氯化钠的饱和溶液中加入硝酸钾 | C.向混有少量硫酸的硫酸铜溶液中加入氢氧化钠溶液 | D.向一定质量的稀盐酸中加氢氧化钠 |
A. A B. B C. C D. D
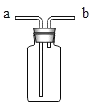
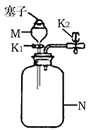
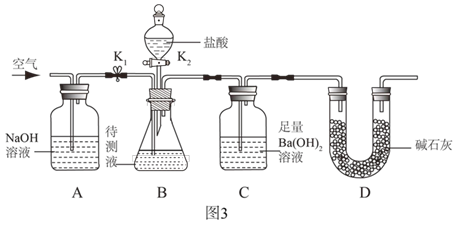
【题目】在高温下,铁与水蒸气能发生反应生成一种常见的铁的氧化物和一种气体。某兴趣小组请你参与研究:铁与水蒸气反应一段时间后剩余固体物质的成分、性质和利用。实验装置如下图所示(夹持仪器略)
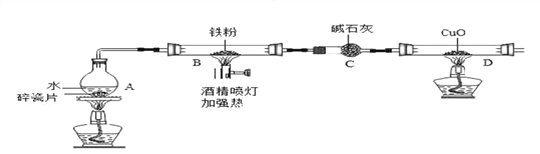
(推断) 观察到D中的黑色固体变红,则B中生成的气体是_______;
(实验探究) B装置中的剩余固体是什么?
(查阅资料)(1)碎瓦石能防止爆沸,碱石灰是氧化钙和氢氧化钠的混合物;
(2)铁的氧化物中,只有Fe2O3是红棕色,其余均为黑色,只有Fe3O4能被磁铁吸引;
(初步探究) B装置中剩余固体为黑色,能全部被磁铁吸引
(猜想和假设)
猜想一:剩余固体是Fe3O4;
猜想二:剩余固体是___________;
(实验探究)
实验操作 | 实验现象 | 实验结论 |
取少量黑色固体于试管中,加入足量的稀盐酸; | ____________ | 则猜想二正确 |
(实验结论)铁与水蒸气反应的化学方程式为_________________________________。
(成分再利用)若将B装置中剩余的黑色固体ag,经过一系列转化,全部变为红棕色固体Fe2O3(假设转化过程中铁元素无损耗),增加的质量为x,则x的取值范围为_____________。(用a来表示,精确到0.01)