题目内容
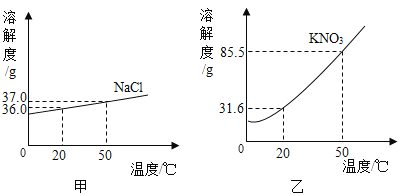
【题目】根据如图所示的KNO3和NaCl的溶解度曲线,回答下列问题。
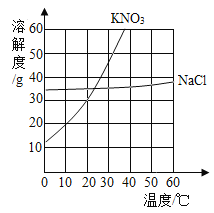
(1)10°C时,KNO3的溶解度约是_____g;
(2)NaCl溶液中含有少量KNO3,提纯NaCl采用的方法是_____(选填“蒸发结晶”或“降温结晶”);
(3)将20°C的KNO3饱和溶液升温至60°C,以下说法正确的是_____。
A溶质的质量分数不变
B溶解度不变
C溶质的质量不变
【答案】20 蒸发结晶 AC
【解析】
(1)由图可知,10°C时,KNO3的溶解度约为20g,故填20。
(2)由图可知,氯化钠与硝酸钾的溶解度均随温度升高而增大,但氯化钠的溶解度受温度影响较小,如果氯化钠溶液中混有少量的硝酸钾,提纯氯化钠应采用蒸发结晶的方法将氯化钠从其饱和溶液中结晶析出,故填蒸发结晶。
(3)A 由图可知,硝酸钾的溶解度随温度升高而增大,将20°C的KNO3饱和溶液升温至60°C,硝酸钾的溶解度增大,溶液由饱和溶液变为不饱和溶液,溶液中的溶质与溶剂的质量不变,则溶液中溶质的质量分数不变,选项正确;
B 由图可知,硝酸钾的溶解度随温度升高而增大,将20°C的KNO3饱和溶液升温至60°C,硝酸钾的溶解度增大,选项错误;
C 由图可知,硝酸钾的溶解度随温度升高而增大,将20°C的KNO3饱和溶液升温至60°C,硝酸钾的溶解度增大,溶液由饱和溶液变为不饱和溶液,溶液中溶质的质量不变,选项正确,故填AC。

【题目】黄铜是一种重要的金属,它是铜和锌的合金,可用来制造机器、电器零件及日常用品。为了测定黄铜样品的组成,取五份样品分别加稀硫酸反应,其实验数据记录如下:
样品 | 第1份 | 第2份 | 第3份 | 第4份 | 第5份 |
取样品质量(g) | 40.0 | 40.0 | 40.0 | 40.0 | 40.0 |
取稀硫酸质量(g) | 30.0 | 60.0 | 90.0 | 120.0 | 150.0 |
产生气体质量(g) | 0.3 | 0.6 | 0.9 | 1.0 | 1.0 |
按要求回答下列问题:
(1)根据实验数据分析,从第________份开始,金属已经反应完全了。
(2)列式计算该黄铜样品中金属锌的质量分数。(要求写出计算过程)