题目内容
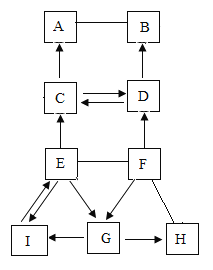
【题目】如图中A-I是初中化学常见的物质,且分别是由H、O、S、Cl、Ca、Cu中的一至三种元素组成。其中D、I为单质;C、E为氧化物;其余物质类别属于酸、碱、盐。A可用于改良酸性土壤。固体G呈白色,其溶液显蓝色。图中“—”表示两端的物质间能发生化学反应:“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去。
(1)写出化学式:A_____,G_____。
(2)写出D→B反应的化学方程式_____。
(3)写出F—H反应的化学方程式_____。
【答案】Ca(OH)2 CuSO4 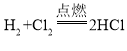
![]()
【解析】
A可用于改良酸性土壤,可推出A为氢氧化钙,C为氧化物,且C能转化为氢氧化钙,D为单质,C能与D 相互转化,D能转化为B,且B能与氢氧化钙反应,B属于酸、碱、盐,可推出C为水,D为氢气,B为HCl;固体G呈白色,其溶液显蓝色,可推出G为硫酸铜,G能转化为I,I为单质,可推出I为铜,I能与E相互转化,E为氧化物,可推出E为氧化铜,氧化铜能与F反应转化为硫酸铜,可推出F为硫酸,硫酸铜能转化为H,且H能与硫酸反应,可推出H为氢氧化铜,代入验证,符合题意。
(1)A为氢氧化钙,化学式为:Ca(OH)2,G为硫酸铜,化学式为:CuSO4;
(2)D为氢气,B为HCl,氢气在氯气中燃烧生成氯化氢,该反应的化学方程式为: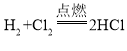 ;
;
(3)F为硫酸,H为氢氧化铜,氢氧化铜与硫酸反应生成硫酸铜和水,该反应的化学方程式为:![]() 。
。

 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案【题目】为测定锌铜合金中锌的含量,取该合金放入如图 14 盛有稀硫酸的锥形瓶中,发生反应: Zn+H2SO4=ZnSO4+H2↑ 。多次实验后,取平均值所得数据如下表:

反应前 | 充分反应后装置及反应剩余物质质量 | |
装置和足量的稀硫酸质量 | 锌铜合金质量 | |
342.10g | 16.00g | 357.70g |
若不考虑干燥剂吸收空气中的水蒸气,计算:
(1)根据质量守恒定律求生成氢气的质量。
(2)该合金中锌的质量分数。