题目内容
【题目】某化学实验小组的同学作了如下实验,向点滴板上加入氢氧化钠溶液和氢氧化钙溶液,然后向氢氧化钠溶液中加入几滴酚酞溶液,向氢氧化钙溶液中加入一定量的稀盐酸,如图所示。
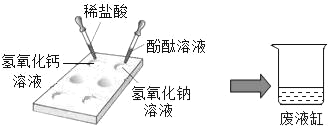
请你写出氢氧化钠溶液中加入酚酞溶液的现象(1)_____;
氢氧化钙溶液中加入稀盐酸的化学方程式(2)_____;
实验后同学们将所有的废液全部倒入废液缸中发现废液为无色,这一现象引起了同学们的注意,他们决定对废液缸中的成分进行探究。
(提出问题):废液缸中的溶质是什么?(除酚酞以外)
(猜想与假设):童童同学认为:NaCl CaCl 2 HCl
婷婷同学认为:NaCl CaCl 2 Ca(OH)2
小宇同学认为:NaCl CaCl 2;
(交流与评价):你认为(3)_____同学的猜想是错误的,原因(4)_____;
童童同学为了证明自己的猜想,取少量废液于试管中,加入(5)_____观察到(6)_____现象,证明自己的猜想是正确的。 此探究实验中用到了点滴板,点滴板的优点是(7)_____。
【答案】无色溶液变为红色 Ca(OH)2+2HCl=CaCl2+2H2O 婷婷 溶液无色,说明溶液不显碱性,一定没有Ca(OH)2 加入石蕊溶液 溶液由紫色变为红色 节约药品,便于对比
【解析】
氢氧化钠溶液显碱性,能使无色酚酞变红色,所以出氢氧化钠溶液中加入酚酞溶液的现象是:无色溶液变为红色;
氢氧化钙和盐酸反应生成氯化钙和水,化学方程式为:Ca(OH)2+2HCl=CaCl2+2H2O;
[交流与评价]酚酞遇碱变红色,所以婷婷同学的猜想是错误的,原因:溶液无色,说明溶液不显碱性,一定没有Ca(OH)2;
酸能使紫色石蕊变红色,以及点滴板便于比较实验现象,所以取少量废液于试管中,加入加入石蕊溶液观察到溶液由紫色变为红色现象,证明自己的猜想是正确的。 此探究实验中用到了点滴板,点滴板的优点是:节约药品,便于对比。
故答案为:(1)无色溶液变为红色;
(2)Ca(OH)2+2HCl=CaCl2+2H2O;
[交流与评价](3)婷婷错误;
(4)溶液无色,说明溶液不显碱性,一定没有Ca(OH)2;
(5)加入石蕊溶液;
(6)溶液由紫色变为红色;
(7)节约药品,便于对比。