题目内容
【题目】利用下图装置测定空气中氧气含量,实验步骤如下(装置气密性良好,部分操作已略去,因导管产生的误差忽略不计):
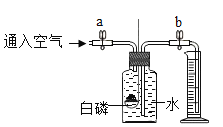
(1)打开止水夹a、b,向集气瓶中缓慢通入一定量的空气,通入集气瓶内空气的量应该满足的条件是____,测得进入量筒中水的体积为V1。
(2)关闭止水夹a、b,用强光照射引燃白磷,发生反应的化学方程式是_______。
(3)白磷熄灭并冷却至室温,打开b,看到的现象是________,测得量筒内水的体积是V2。根据实验记录V1、V2,得出空气中氧气的体积分数的计算式是_________。
【答案】盛有白磷的燃烧匙在水面上方 4P+5O2![]() 2P2O5 量筒内的水进入集气瓶(或水倒吸进入瓶中)
2P2O5 量筒内的水进入集气瓶(或水倒吸进入瓶中) ![]()
【解析】
(1)打开止水夹a、b,向集气瓶中缓慢通入一定量的空气,通入集气瓶内空气的量应该满足的条件是白磷必须与氧气接触才可以燃烧,才能消耗氧气。故填:盛有白磷的燃烧匙在水面上方。
(2)关闭止水夹a、b,用强光照射引燃白磷,发生反应的化学方程式为: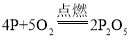 。故填:
。故填: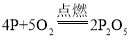 。
。
(3)白磷熄灭并冷却至室温,打开b,因为集气瓶中的氧气被消耗,冷却后压强减小,所以会看到量筒中的水沿导管进入集气瓶中;打开止水夹a、b,向集气瓶中缓慢通入一定量的空气,测得进入量筒中水的体积为V1,V1就是进入集气瓶中空气的体积,反应结束后量筒中的水进入集气瓶后,测得量筒内水的体积是V2,量筒中水减少的体积就是消耗的氧气体积(V1- V2),得出空气中氧气的体积分数的计算式是:![]() 。故填:量筒内的水进入集气瓶(或水倒吸进入瓶中);
。故填:量筒内的水进入集气瓶(或水倒吸进入瓶中);![]() 。
。

 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
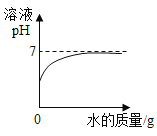
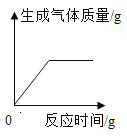
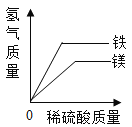
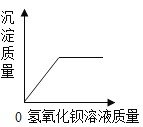
教育世家状元卷系列答案【题目】下列各选项与如图所示曲线相符的是
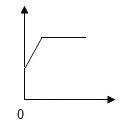
选项 | 实验操作 | 横坐标 | 纵坐标 |
A | 向一定质量的锌粉中加入稀硫酸 | 加入稀硫酸的质量/g | 生成氢气的质量/g |
B | 向一定质量的硝酸银溶液中加入铜粉 | 加入铜粉的质量/g | 溶液的质量/g |
C | 向一定质量的稀盐酸中不断加入碳酸钙粉末 | 加入碳酸钙的质量/g | 溶液的质量/g |
D | 向氯化钠饱和溶液中加入水 | 加入水的质量/g | 溶质的质量/g |
A.AB.BC.CD.D
【题目】下列实验方案不能达到实验目的的是
选项 | 实验目的 | 实验方案 |
A | 配制50 g 6%的氯化钠溶液 | 称取3 g氯化钠固体溶于47 mL水中 |
B | 鉴别硬水和软水 | 加入肥皂水,振荡,观察现象 |
C | 除去铜粉中少量的木炭 | 将混合物在空气中灼烧 |
D | 除去NaOH溶液中少量的Na2CO3 | 加入适量的Ca(OH)2溶液,充分反应后过滤 |
A.AB.BC.CD.D
【题目】某化学课堂正在进行,请你参与他们的学习并完成相关任务。
[演示实验]老师按图示连接好装置,加入NaHCO3粉末,点燃酒精灯,对试管预热后集中加热,烧杯中澄清石灰水变浑浊,说明生成了CO2 ,继续加热至无气体产生后撤出导管,熄灭酒精灯。
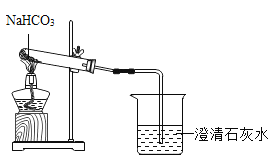
[提出问题]实验结束后,同学们对试管中剩余的固体粉末产生了兴趣。剩余的固体粉末由什么物质组成?
[猜想假设]在老师的指导下,同学们对固体粉末做出如下猜想:
猜想一:NaOH;
猜想二:_____;
猜想三:Na2CO3.
[实验探究]
(1)方案一:
取适量粉末溶于水中,向溶液中滴入2滴无色酚酞溶液,摇匀,观察到溶液由无色变为红色。小明根据实验现象判断猜想一成立。 小组讨论后,大家认为小明的结论不合理,理由是_____。
(2)方案二:
实验操作 | 实验现象 | 实验结论 | |
步骤一 | 取适量粉末溶于水后加入过量的BaCl2溶液 | ____ | 猜想一不成立 |
步骤二 | 取步骤一的上层清液,向其中加入2~3 ml. MgCl2溶液 | 无明显现象 | 猜想____成立 |
[评价交流]小华认为步骤二也可以用MgSO4溶液代替MgCl2溶液,大家不同意他的观点,理由是____。
[拓展延伸]请你根据上述实验成果,写出碳酸氢钠受热分解的化学方程式:_____。