题目内容
【题目】水是生命之源,“珍惜水、节约水、保护水”是每个公民的义务和责任。
(1)下列“水”属于纯净物的是______(填标号)
A.蒸馏水
B.河水
C.自来水
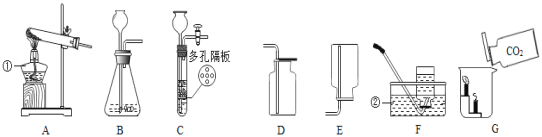
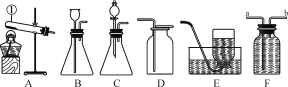
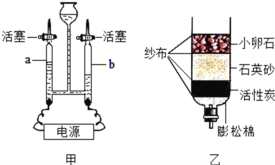
(2)用图中的甲装置进行电解水的实验,b管中收集到的气体是_____(填物质名称),写出该反应的化学方程式_______________。该实验说明:从宏观上看,水是由________组成的;从微观上看,水是由_____构成的。
(3)某同学自制如图中乙所示简易净水器,其中活性炭起到 _________作用。
(4)人们常用________检验地下水是硬水还是软水;生活中可用______的方法降低水的硬度。
(5)高铁酸钾(K2FeO4)是一种新型、高效的多功能水处理剂。高铁酸钾溶于水时发生了以下反应:4K2FeO4+10H2O===4Fe(OH)3+8KOH+3R↑,则R是____________(填化学式)。
(6)请举一例生活中节约用水的具体措施 ____________。
【答案】A 氢气 2H2O![]() 2H2↑+O2↑ 氢元素和氧元素 水分子 吸附 肥皂水 煮沸 O2 用淘米的水洗菜(随手关掉水龙头等合理答案均可)
2H2↑+O2↑ 氢元素和氧元素 水分子 吸附 肥皂水 煮沸 O2 用淘米的水洗菜(随手关掉水龙头等合理答案均可)
【解析】
(1)混合物是由两种或两种以上的物质组成,河水、自来水都属于混合物;纯净物是由一种物质组成,蒸馏水中只有水分子,属于纯净物,故选A。
(2)甲装置进行电解水的实验,反应方程式为2H2O![]() 2H2↑+ O2↑,根据氧气与氢气体积的多少和气体的检验,b中收集到的较多的气体是氢气,氢气能够燃烧,具有可燃性;该实验说明从宏观上看,水是由氢元素和氧两种元素组成的;从微观上看,水是由水分子构成的,每一个水分子是由两个氢原子和一个氧原子构成的。
2H2↑+ O2↑,根据氧气与氢气体积的多少和气体的检验,b中收集到的较多的气体是氢气,氢气能够燃烧,具有可燃性;该实验说明从宏观上看,水是由氢元素和氧两种元素组成的;从微观上看,水是由水分子构成的,每一个水分子是由两个氢原子和一个氧原子构成的。
(3)活性炭有吸附作用,能吸附一些杂质、色素、异味等。
(4)区分硬水和软水的方法是:用肥皂水,加入肥皂水,泡沫多的是软水,泡沫少的是硬水;在生活中常用加热煮沸的方法降低水的硬度。
(5)根据质量守恒定律可知,化学反应前后元素种类不变,原子种类、个数不变,故推出R为O2。
(6)生活中节约用水的具体措施有:用淘米水浇花浇菜、用洗衣服的水冲马桶、随手关掉水龙头等。

【题目】实验室可利用碱式碳酸铜(化学式:Cu2(OH)2CO3)制备氧化铜,并进行碳粉还原氧化铜的实验。
查阅资料:烧碱固体有吸水性且能与二氧化碳发生反应。
无水硫酸铜遇水会由白色变成蓝色。
①制备氧化铜并检验产物,装置如图所示(省略夹持仪器):
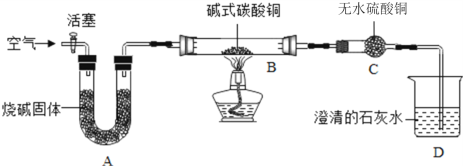
步骤一:连接A和B,打开活塞,通入空气。
步骤二:关闭活塞,连上C和D开始加热。观察到C中固体变蓝,D中澄清石灰水变浑浊。
步骤三:在加热过程中,记录在B中固体质量变化如下表,在t3时停止加热。
加热时间(min) | 0 | t1 | t2 | t3 |
B中固体质量(g) | 6.66 | 5.20 | 4.80 | 4.80 |
①B中发生反应的化学方程式为:__________ , A的作用是吸收空气中的_______,防止对产物检验造成干扰。选择t3时停止加热的理由是____________。
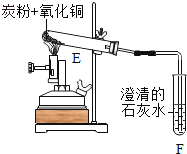
②一定量碳粉还原①中制得的氧化铜并检验产物,装置如图所示:写出该反应的化学方程式________,实验过程中,观察到F中溶液变浑浊,E中的现象是___________反应完全后,若仅撤走酒精喷灯停止加热,可能导致的后果是____________
③若①中省略步骤三,对②中反应产物判断可能产生的影响及其原因______________。
④计算②反应后理论上可制得多少克铜__________。