题目内容
【题目】小红同学向盐酸与氯化钡的混合溶液中逐滴滴入碳酸钠溶液至过量,记录滴入的碳酸钠溶液的质量(x)与有关量的变化关系如图所示,下列判断正确的是
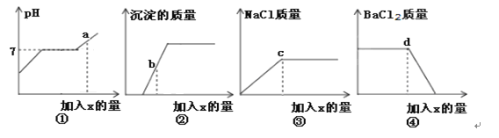
A.①图中,当碳酸钠溶液加至a点时,溶液中Na2CO3正与BaCl2发生反应
B.②图中,当碳酸钠溶液加至b点时,所得溶液的pH=7
C.③图中,当碳酸钠溶液加至c点时,溶液中含有的溶质是氯化钠和氯化钡
D.④图中,当碳酸钠溶液加至d点时,溶液中BaCl2与Na2CO3恰好反应完全
【答案】B
【解析】】
试题分析:A.当碳酸钠溶液加至a点表示碳酸钠与氯化钡恰好完全反应后继续加入碳酸钠至过量,,碳酸钠溶液呈碱性,pH大于7,pH不再发生变化,错误;B、b点表示稀盐酸和碳酸钠完全反应后,氯化钡和碳酸钠反应生成沉淀的情况,由于沉淀没有达到最大值,溶液中既没有盐酸,也没有剩余的碳酸钠,而溶液中只有氯化钡和氯化钠,此时所得溶液呈中性,pH等于7,正确;C、c点表示氯化钠的最大值,稀盐酸和碳酸钠,氯化钡和碳酸钠反应都生成氯化钠,所以当氯化钠为最大值时,溶液中也一定没有稀盐酸和氯化钡,错误;D、d点表示表示氯化钡质量逐渐减少的点,所以此时是稀盐酸和碳酸钠刚好完全反应,而氯化钡和碳酸钠也开始反应,错误。故选B

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
【题目】小明同学对所学部分化学知识归纳如下,其中有错误的一组是
A.物质用途 | B.安全常识 |
稀有气体——焊接金属的保护气 乙二醇——汽车水箱防冻液 | 煤气泄漏——关闭气阀、严禁烟火 电器着火——用液态二氧化碳灭火器 |
C.元素与人体健康 | D.生活经验 |
缺碘——会得甲状腺疾病 缺锌——骨质疏松,易得佝偻病 | 区别CO和CO2——澄清石灰水 鉴别氧气和氮气——带火星的木条 |