题目内容
【题目】化学是一门以实验为基础的科学。请回答:
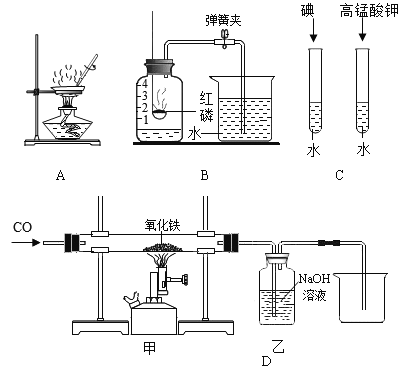
(1)A实验中玻璃棒的作用是___________;
(2)B实验中导致实验结果偏小的原因是_____(写一个);
(3)C实验的目的是___________;
(4)关于D实验,下列说法正确的是 ___________(填字母)。
A加热前应先通入一氧化碳以排尽装置内的空气
B加热一段时间后,甲玻璃管内黑色粉末变成红色
C该实验需要添加尾气处理装置
D乙装置可以用来检验反应中产生的CO2气体
【答案】搅拌,防止局部温度过高造成液滴飞溅 红磷量不足等合理答案 比较不同溶质在相同溶剂里的溶解性 A
【解析】
(1)A实验是蒸发操作,玻璃棒的作用是搅拌,防止局部温度过高造成液滴飞溅。故填:搅拌,防止局部温度过高造成液滴飞溅;
(2)B实验中导致实验结果偏小的原因有:①红磷的量不足;②装置漏气(在冷却过程中有外界的空气进入瓶中);③未等到装置冷却至室温就打开了弹簧夹,并进行读数(因为此时剩余的气体在受热状态下,处于膨胀状态,占据了部分水的体积);
故填:红磷量不足等;
(3)C实验中高锰酸钾能溶于水,碘不能溶于水,C实验的目的是比较不同溶质在相同溶剂里的溶解性。故填:比较不同溶质在相同溶剂里的溶解性;
(4)A、加热前应先通入一段时间的CO以排尽装置内的空气,防止加热时发生爆炸,故选项说法正确。
B、一氧化碳具有还原性,能与氧化铁反应生成铁和二氧化碳,实验进行一段时间后,玻璃管中出现的现象是红棕色粉末逐渐变黑,故选项说法错误。
C、该装置不需要添加尾气处理装置,是因为多余的CO已收集在乙中,故选项说法错误。
D、氢氧化钠与二氧化碳反应生成碳酸钠和水,但无明显现象,NaOH溶液应改为Ca(OH)2溶液以检验产生的CO2气体,故选项说法错误。
故选:A。

【题目】下表是Ca(OH)2和NaOH的溶解度数据。请回答下列问题:
温度/°C | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/(g/100g水) | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
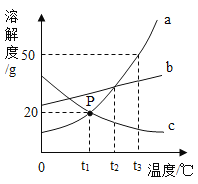
①依据上表数据,绘制Ca(OH)2和NaOH的溶解度曲线,下图中表示NaOH溶解度曲线的是_____(填A或B)。
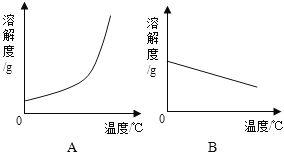
②把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有_____。(填一种)
③20℃时,191g饱和NaOH溶液,恒温蒸发10g水后,可析出NaOH晶体_____g。
④现有60°C时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是_____。
⑤20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH_____(填“偏大”、“偏小”或“不受影响”)。
【题目】为探究盐酸的化学性质,某化学小组做了如下实验:
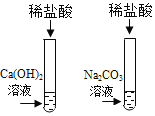
将反应后两只试管中的废液倒入一个洁净的烧杯中,观察到烧杯中先有气泡产生,后有白色沉淀出现。将烧杯中的混合物过滤,得到白色沉淀和无色滤液。同学们对滤液中溶质的成分进行探究。
[提出问题]滤液中溶质的成分是什么?
[假设与猜想]猜想一: NaCl
猜想二: NaCl 和CaCl2
猜想三: NaCl、Ca(OH)2 和HCl
猜想四:___________。
[讨论与交流]经讨论同学们一致认为猜想_________是错误的。原因是____________(用化学方程式解释)
[实验与结论]
实验步骤 | 实验现象 | 实验结论 |
取少量滤液于试管中,滴加适量碳酸钠溶液 | 无现象 | 猜想四成立 |
取少量滤液于试管中,滴加适量_______________ | ______________________ |
[拓展与迁移]稀盐酸和稀硫酸有相似的化学性质,是因为它们的溶液中都存在_______________。
【题目】为制取干燥的二氧化碳气体,并验证二氧化碳气体与氢氧化钠溶液可以发生化学反应,设计如下探究实验
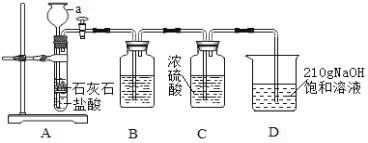
(资料)①碳酸钠、水、二氧化碳可以化合生成碳酸氢钠。
②20℃时,氢氧化钠、碳酸钠和碳酸氢钠的溶解度如下表所示。
物质 | NaOH | Na2CO3 | NaHCO3 |
溶解度/g | 110 | 21.8 | 9.6 |
假设:实验过程中装置D的温度维持在20℃,请根据设计的装置和资料回答问题:
(定性探究)
(1)仪器a的名称是_____________,要使A中反应停止,最简便的操作方法是__________________。
(2)装置B中盛有 NaHCO3溶液,作用是吸收装置A中挥发出的HC气体,B中发生反应的基本反应类型是____________反应(选填:“化合”、“分解”、“置换”、“复分解”)。
(3)装置C的作用是________________________________________。
(4)在实验过程中装置D中观察到______________________________,说明CO2和NaOH溶液能发生反应,当通入装置D中的CO2过多时,还会与Na2CO3化合成 NaHCO3,该反应的化学方程式是_________________________。