题目内容
【题目】属于化学变化的是
A.食物变质 B.冰雪融化 C.海水晒盐 D.衣服晾干
【答案】A
【解析】
试题分析:有新物质生成即物质种类改变的属于化学变化。A、食物变质有新物质生成,属于化学变化;B、物质状态改变,没有生成新物质,属于物理变化;C、通过蒸发溶剂使溶质析出,物质状态改变,没有生成新物质,属于物理变化;D、衣服上的水蒸发,物质状态改变,没有生成新物质,属于物理变化。

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案
相关题目
【题目】下列有关分子原子的观点正确的是( )
选项 | 事实 | 解释 |
A | 氧分子比氮原子大 | 分子一定比原子大 |
B | 10毫升水和10毫升水混合,无明显变化 | 分子之间没有间隔 |
C | 水电解是化学变化 | 水分子本身发生改变,变成其他物质的分子 |
D | 水分子不显电性 | 水分子中没有带电的粒子 |
【题目】溶液在生产、生活中起着十分重要的作用。请回答下列问题:
(1)可以作为溶质的是_________。
A.只有固体 B.只有液体 C.只有气体 D.气体、液体、固体都可以
(2)配制100g质量分数为16%的氯化钠溶液,所需氯化钠的质量为________,水的体积为________mL (水的密度近似看作1g/cm3)。
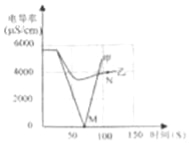
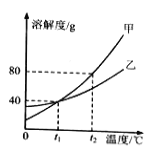
(3)甲、乙两种不含结晶水的固体物质的溶解度曲线如右下图.t1℃时,甲物质的溶解度是________。t2℃时,若从甲和乙两种物质的饱和溶液中析出等质量的固体,须蒸发掉较多水的是________(填“甲”或“乙”)物质的饱和溶液。
选项 | x | y |
A | 水 | 氧化钙 |
B | 水 | 硝酸铵 |
C | 浓硫酸 | 水 |
D | 稀盐酸 | 镁 |
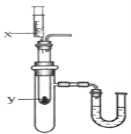
(4)按右上图所示装置,将液体X注入装有固体y的试管中,会导致U形管中右端液面升高。则可能的组合是______。