题目内容
【题目】某科研小组设计利用稀硫酸浸取某废弃的氧化铜锌矿(主要成分为CuO和ZnO,其余成分既不与酸反应,也不溶于水)的方案,实现废物综合利用。部分流程如下:
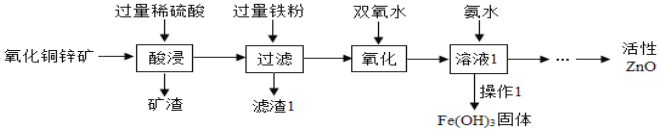
请回答:①操作1的名称是_____;
②步骤“酸浸”中发生化学反应的化学方程式为_____、_____;
③加入过量铁粉后,反应的基本反应类型是_____,得到的滤渣1的成分的化学式为_____;
④在实验过程中双氧水会与Fe2+反应成Fe3+和水,以便在后续的操作中将溶液中的铁元素除去。高锰酸钾溶液也能将Fe2+氧化成Fe3+,同时生成可溶性的锰盐。选用双氧水的优点是_____。
【答案】过滤 CuO+H2SO4==CuSO4+H2O ZnO+H2SO4==ZnSO4+H2O 置换反应 Fe和Cu 产物是水,不会带来新的杂质
【解析】
(1)操作1是将液体和固体分离的操作,是过滤;
(2)氧化铜锌矿的主要成份是氧化铜和氧化锌,金属氧化物与酸反应生成盐和水,其反应的化学方程式为:ZnO+H2SO4═ZnSO4+H2O,CuO+H2SO4=CuSO4+H2O;
(3)加过量铁粉后,发生的反应是铁和硫酸铜的反应,生成铜和硫酸亚铁,符合置换反应的特征,由于铁粉过量,所以滤渣1的成份是铁和铜;
(4)除杂实验过程中,要注意不要引入新的杂质,特别是难除去的杂质,双氧水只含有氢和氧两种元素,会与Fe2+反应生成Fe3+和水,而不引入难除掉的其它杂质。

练习册系列答案
相关题目