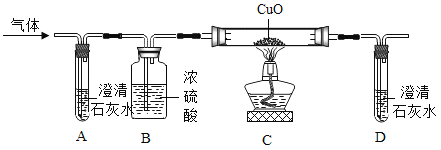
题目内容
【题目】归纳总结是学习化学的重要方法,某化学兴趣小组学习碱的性质后,通过实验对氢氧化钙的化学性质进行了验证和总结,如图所示“﹣﹣”表示物质两两之间能发生化学反应.请根据如图,回答问题,(已知:CaCl2溶液呈中性,CaCl2+Na2CO3═CaCO3↓+2NaCl)。

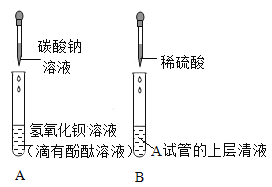
(1)甲同学将酚酞试液滴入氢氧化钙溶液中,然后观察到溶液变红,得出结论:氢氧化钙溶液呈_____(填“酸性”、“碱性”或“中性”);
(2)乙同学将过量的稀盐酸加入到甲同学所得溶液中,观察到的现象是__________,此时所得溶液中含有的溶质有_____________(酸碱指示剂除外);
(3)丙同学将碳酸钠溶液加入氢氧化钙溶液中,充分反应后,与乙同学所得溶液混合,静置后发现:上层为无色透明的溶液,底部有白色沉淀.则上层溶液中一定含有的溶质是__(酸碱指示剂除外),可能含有的溶质是_____。
【答案】碱性 溶液由红色变为无色 氯化钙、氯化氢 氯化钠 氯化钙
【解析】
(1)碱性溶液使酚酞变为红色,酸性、中性溶液都不能使酚酞溶液变色,甲同学将酚酞试液滴入氢氧化钙溶液中,观察到溶液变红,可以得出结论:氢氧化钙溶液呈碱性;
(2)乙同学将过量的稀盐酸加入到甲同学所得溶液中,氢氧化钙与稀盐酸反应生成氯化钙和水,已知CaCl2溶液呈中性,盐酸过量,最终溶液为中性,不能使酚酞变色,溶液由碱性变为酸性,观察到的现象是溶液由红色变为无色,此时所得溶液中含有的溶质有氯化钙和氯化氢;
(3)丙同学将碳酸钠溶液加入氢氧化钙溶液中,碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,二者反应结果未知,充分反应后,与乙同学所得溶液混合,乙同学所得溶液为酚酞、氯化钙和稀盐酸的混合溶液,已知碳酸钠与稀盐酸反应生成氯化钠、二氧化碳和水,氢氧化钠与稀盐酸反应生成氯化钠和水,碳酸钠与氯化钙反应生成氯化钠和碳酸钙,碳酸钠、氢氧化钠、氢氧化钙的溶液均呈碱性,能使酚酞溶液变红,静置后发现:上层为无色透明的溶液,底部有白色沉淀,因为含有酚酞,不会有氢氧化钠、氢氧化钙、碳酸钠,底部有白色沉淀,说明稀盐酸已经完全反应,则上层溶液中一定含有的溶质是氯化钠,可能含有的溶质是氯化钙。

【题目】Cl2是黄绿色气体,水溶液叫氯水,把品红试纸伸入氯水中,品红试纸褪色。
[提出问题]氯水中的哪些成分能使品红试纸褪色呢?
[查阅资料]氯气溶于水,部分与水反应,方程式为![]() 。HClO(次氯酸)是一种弱酸,具有强氧化性。
。HClO(次氯酸)是一种弱酸,具有强氧化性。
[猜想假设]猜想1:氯水中的水使品红褪色;猜想2:氯水中的Cl2使品红褪色;
猜想3:氯水中的__使品红褪色;猜想4:氯水中的HClO使品红褪色。
[实验探究]
实验操作 | 实验现象 | 实验结论 |
1.把品红试纸伸入水中 | 没有褪色 | 猜想1__ |
2.____ | 没有褪色 | 猜想2不成立 |
3.把品红试纸伸入稀盐酸中 | _ | 猜想3不成立 |
[实验结论]综合分析判断:氯水中的__(填化学式)使品红褪色,具有漂白作用(能使品红等有色物质褪色)。
[拓展应用]①向氯水中滴加紫色石蕊溶液,观察到的现象是___;②氯水中加人AgNO3溶液有白色沉淀生成,化学方程式为__。
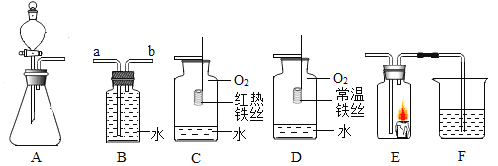
【题目】CaO和NaOH固体的混合物,俗名“碱石灰”,实验室常用作干燥剂.碱石灰在空气久置会吸收空气中的水和二氧化碳而变质.某实验小组为确定一瓶久置的碱石灰样品的成分,设计了图所示实验流程.
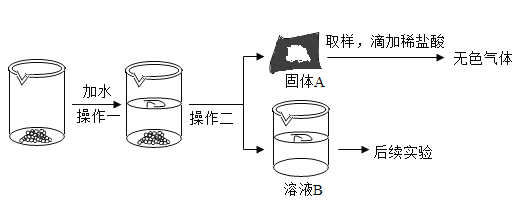
请你参与探究过程:
(1)为了使样品充分溶解,操作一中还要用到的玻璃仪器是__;操作二的名称是__.
(2)固体A中一定含有__.
(3)溶液B成分的探究.
(查阅资料)
①Ca(OH)2、Na2CO3溶于水无明显的温度变化;
②Na2CO3溶液呈碱性,能使酚酞试液变红;
③CaCl2溶液呈中性且能与碳酸钠发生复分解反应.
(猜想)溶液B中溶质可能为:①NaOH ②Na2CO3③NaOH和Na2CO3④Ca(OH)2和__
(设计方案并进行实验)甲、乙同学分别设计如下方案并进行探究:
甲同学:取少量溶液B于试管中,滴加足量的稀盐酸,产生大量气泡,则溶液B中的溶质是Na2CO3.
乙同学:取少量溶液B于试管中,滴加几滴酚酞试液,溶液变成红色,则溶液B中的溶质一定含有NaOH.丙同学认真分析上述二位同学的实验,认为他们的结论均有不足之处,并且做出了正确的判断.他认为B溶液中一定含有Na2CO3,可能含有NaOH.为进一步确认溶液B中是否含NaOH,他做了如下实验.
实验步骤 | 实验现象 | 实验结论 |
①取少量溶液B于试管中,加入足量CaCl2溶液; ②过滤,在滤液中滴加酚酞试液 | __ | 猜想③正确 |
实验步骤①的目的是__.
(4)实验过程中,同学们发现向样品中加水时还放出大量的热.综合以上探究,下列对样品成分分析正确的是__(填序号).
A 一定有
B 一定有Na2CO3
C 一定有CaO
D 至少有NaOH、CaO中的一种.