题目内容
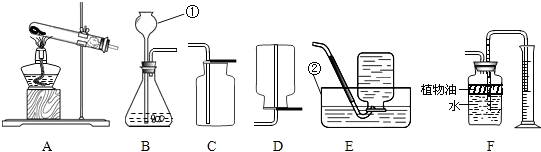
如图所示装置可用来测定空气中氧气的含量.对该实验认识不正确的是

- A.白磷的量不足会影响实验结论
- B.装置不漏气是实验成功的重要因素之一
- C.将白磷改为木炭也能得到正确的实验结论
- D.试管内压强的减小会导致试管内液面上升
C
分析:利用实验室测定氧气的实验正确操作中注意的问题作出选择,正确操作才能保证实验成功,然后据题中信息分析即可,消耗氧气使试管内压强减小,水倒吸入试管内.
解答:A、红磷的量不足不能消耗完瓶内氧气,进入的水减少会影响实验结论,故A说法正确;
B、如果装置漏气进入的水会减少,所以装置不漏气是实验成功的重要因素之一,故B说法正确;
C、由于木炭燃烧生成二氧化碳也是气体,所以瓶内压强基本保持不变,所以水不会进入,所以换成木炭不行,故C说法错误;
D、由于白磷燃烧消耗了氧气,使试管内气体压强的减小,会导致试管内液面上升,故D说法正确.
故选C.
点评:解答本题的关键是要知道测定空气中氧气的含量的原理和实验注意事项.
分析:利用实验室测定氧气的实验正确操作中注意的问题作出选择,正确操作才能保证实验成功,然后据题中信息分析即可,消耗氧气使试管内压强减小,水倒吸入试管内.
解答:A、红磷的量不足不能消耗完瓶内氧气,进入的水减少会影响实验结论,故A说法正确;
B、如果装置漏气进入的水会减少,所以装置不漏气是实验成功的重要因素之一,故B说法正确;
C、由于木炭燃烧生成二氧化碳也是气体,所以瓶内压强基本保持不变,所以水不会进入,所以换成木炭不行,故C说法错误;
D、由于白磷燃烧消耗了氧气,使试管内气体压强的减小,会导致试管内液面上升,故D说法正确.
故选C.
点评:解答本题的关键是要知道测定空气中氧气的含量的原理和实验注意事项.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目

 20、某课外活动小组研究外界条件对水中氧气含量的影响.他们利用仪器测得以下数据.
20、某课外活动小组研究外界条件对水中氧气含量的影响.他们利用仪器测得以下数据.