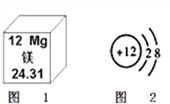
题目内容
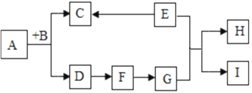
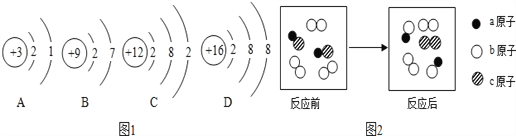
【题目】(1)如图是初中化学中六种常见物质之间的转化关系图。
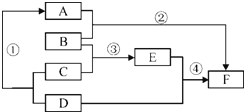
已知A、D、F均为单质,其中D、F为金属单质,D的合金是使用最多的金属材料;B为氧化物,C是一种常见的酸,E(相对分子质量为160)的溶液呈蓝色.试回答下列问题:(框图中的反应条件和某些生成物已略去)
① 请写出下列物质的化学式:B_____,D_____。
② 上述反应中,不属于置换反应的是____(填序号),其反应的化学方程式为________。
③ 请写出反应④的化学方程式:______________________。
④ 请写出E在生产生活中的一种用途_____。
(2)Mg与NH4Cl溶液反应,除生成一种盐外,还有气泡产生。为确定气体的成分,进行下列实验探究:
【假设与猜想】气体可能是HCl,NH3,H2中的一种或几种。
【查阅资料】
①NH3+HCl=NH4Cl
②2NH3+H2SO4=(NH4)2SO4
③2NH3+3CuO![]() 3Cu+N2+3H2O
3Cu+N2+3H2O
【实验探究】
Ⅰ.为确定是否含有HCl,将气体通入酸化的___溶液中,无沉淀产生,则该气体中无HCl。
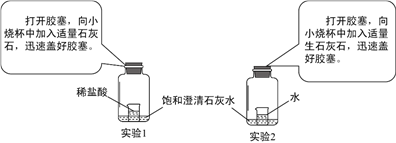
Ⅱ.为了探究其他气体是否存在,又设计了如下实验装置:
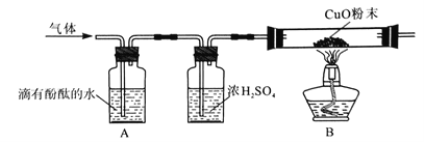
① A中观察到___________________,证明有NH3;
② B中玻璃管内观察到_________证明有H2;
③ 浓硫酸的作用是________。
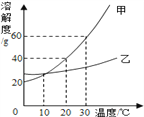
【实验结论】Mg与NH4Cl溶液反应生成盐、NH3和H2。写出化学方程式___________。
【实验反思】综合以上信息和实验结论,有同学认为不需要单独检验HCl,就能证明HCl不存在。请评价这种说法是否合理_____(填“是”或“否”),理由是______。
【答案】 CuO, Fe 。 ③ . CuO+H2SO4= Cu SO4+H2O CuSO4+Fe=Cu+FeSO4 . 制农药等 . AgNO3 溶液变成红色 黑色粉末变成红色 干燥 Mg+2NH4Cl=MgCl2+H2↑+2NH3↑ 是 HCl和NH3.不能共存
【解析】(1)D的合金是使用最多的金属材料,则D是Fe。E(相对分子质量为160)的溶液呈蓝色,则E是CuSO4,B+C→CuSO4,C又是一种常见的酸,则C是H2SO4,CuSO4+Fe=Cu+FeSO4,F为金属单质,F是Cu,C+D→A,C是H2SO4,D是Fe,A为单质,则A是H2,B+C→E,C是H2SO4,E是CuSO4,CuO+H2SO4= CuSO4+H2O,B为氧化物,则B是CuO。① B是CuO,D是Fe。
② 反应①是Fe+ H2SO4 == FeSO4 + H2↑,反应②是H2 + CuO△ Cu + H2O,反应③是CuO+H2SO4= CuSO4+H2O,反应④是CuSO4+Fe=Cu+FeSO4,上述反应中,不属于置换反应的是③。
③ 反应④的化学方程式:CuSO4+Fe=Cu+FeSO4
④ E是CuSO4,在农业生产上可制农药波尔多液。
(2)【实验探究】Ⅰ.氯化氢气体极易溶于水,溶于水所形成的液体是盐酸,HCl+ AgNO3==AgCl↓+ HNO3,无沉淀产生,则该气体中无HCl。Ⅱ.①NH3能使酚酞溶液变红,A中观察到溶液变成红色,证明有NH3;② H2 + CuO△ Cu + H2O,氧化铜是黑色固体,铜是红色固体,B中玻璃管内观察到黑色粉末变成红色,证明有H2;③ 浓硫酸具有吸水性。【实验结论】化学反应前后各种原子个数相等,Mg+2NH4Cl= MgCl2+H2↑+ 2NH3↑【实验反思】NH3是碱性气体,HCl是酸性气体,两者不能共存。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】鸡蛋主要由蛋壳、蛋壳膜、蛋白、蛋黄等几个部分组成,其中蛋壳的主要成分是CaCO3,里面覆盖一层蛋壳膜。化学活动兴趣小组的同学开展了以下探究活动:
【提出问题】蛋壳中的CaCO3含量是多少?

【查阅资料】
a、蛋壳经过科学检测其中含CaCO3的质量分数约为82%~85%,含蛋白质质量分数约14-17%。
b、蛋壳膜中蛋白质含量约为90%~93%。
c、Ba(OH)2是一种碱,化学性质与Ca(OH)2相似。
【设计方案】
方案一:用“灼烧法”,将该蛋壳放在空气中充分灼烧并采集相关数据进行测定。
方案二:用“酸处理法”,将蛋壳与稀盐酸反应后再进行吸收转变为碳酸钡进行测量处理。
【进行实验】
方案一:称取12.0 g蛋壳研磨成粉末置于通风橱中,灼烧至质量不再减少,再称量剩余固体的质量为7.16 g。
方案二:用下图所示的连接实验装置,称取12 g蛋壳样品进行实验(假设其他成分均不与HCl反应,装置内试剂均足量。)
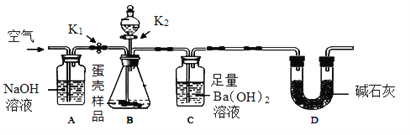
【实验步骤】
① 按上图连接好装置后,并检查装置的气密性;
② 向B装置中加入蛋壳样品后,先通入一会儿空气;
③ 关闭K1,打开K2,向蛋壳样品中滴入10%的盐酸,直到__________为止;
④ 关闭K2,打开K1,再缓缓通入空气一会儿,至装置C中不再产生沉淀为止;
⑤ 将装置C中的固液混合物进行过滤、__________、烘干后称量其质量;
⑥ 重复上述实验。
【数据处理】
方案一:产生的CO2质量__________g,蛋壳中的CaCO3的质量分数为__________%。(保留一位小数)
方案二:重复3次实验,记录数据如下:
实验次数 | 第1次 | 第2次 | 第3次 |
装置C中沉淀质量(/g) | 19.68 | 19.75 | 19.67 |
方案二:实验测得蛋壳中的CaCO3的质量分数__________(写出计算过程,)
(已知:Mr(CaCO3):100 Mr(BaCO3):197)
【评价反思】
(1)方案二中装置D的作用是__________。
(2)方案一测定值与科学检测的数据有较大误差,主要原因是__________。