题目内容
【题目】(1)某元素M的原子结构示意图如图为:
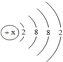
①x的值是__。
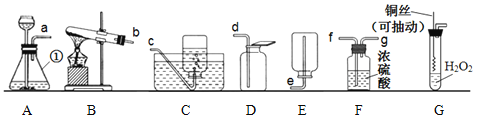
②下列微粒示意图,图1中所表示的元素的化学性质与M元素的化学性质相似的是___(填字母);属于离子的是__(填字母),符号为______。
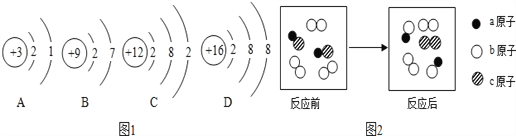
③如图2为某化学反应的微观示意图,其中不同的圆球代表不同的原子,关于该反应,下列说法正确的是__。
A.反应前后分子的种类发生了改变
B.反应前后原子的数目没有增减
C.该反应属于置换反应类型
D.该化学反应生成三种物质
E.参加反应的单质分子与化合物分子的分子个数比为3:2
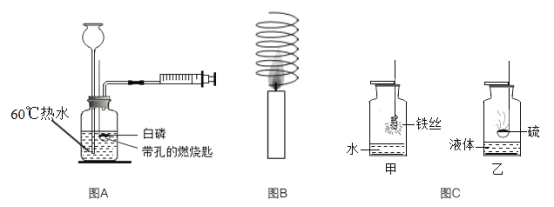
(2)如图表示的是甲、乙两种固体物质的溶解度曲线。
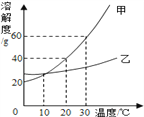
①30℃质量相等的甲、乙两饱和溶液降温到10℃时,甲溶液的质量__乙溶液的质量(填“大于”或“等于”或“小于”);若甲中含有少量乙,应用____________法提纯。
②20℃时,100g水中溶解一定量的甲物质形成饱和溶液,若要把该饱和溶液稀释成质量分数为20%的溶液,应加水__g;实验需要用到的仪器是_________________________。
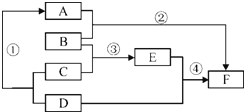
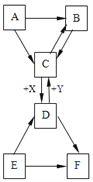
(3)某氯化钾样品含有杂质氯化钙和氯化镁,设计提纯的流程图如下:
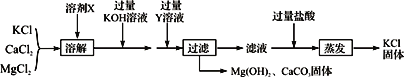
请认真分析流程中各步骤的信息作答:
①溶剂X是____;Y溶液中溶质的化学式为:____。
②蒸发操作的目的是除去(填物质的化学式)____。
③写出加入过量KOH溶液反应的化学方程式:____,其基本反应类型为______。
【答案】 20 C D S2- ABC 小于; 降温结晶或冷却热饱和溶液 60, 玻璃棒、烧杯、100mL量筒、胶头滴管 . 水(或H2O); K2CO3; H2O、HCl(不得有缺); MgCl2+2KOH=Mg(OH)2↓+2KCl; 复分解反应
【解析】(1)①原子中质子数=核外电子数,x=2+8+8+2=20 ②原子的最外层电子个数相同,元素的化学性质相似。质子数≠核外电子数的微粒是离子,质子数为16的原子是硫原子,硫原子易得到2个电子,形成带2个单位负电荷的硫离子S2-。③A.反应前后分子的种类发生了改变,正确;B.反应前后原子的数目没有增减,正确;C.根据反应的微观示意图可知,该反应是一种单质与一种化合物反应,生成另一种单质与另一种化合物,属于置换反应,正确;D.该化学反应生成两种物质,错误;E.参加反应的单质分子与化合物分子的分子个数比为1:2,错误。故选ABC。(2)①甲的溶解度受温度影响比乙大,当30℃质量相等的甲、乙两饱和溶液降温到10℃时,析出甲的质量大于析出乙的质量,故甲溶液的质量小于乙溶液的质量。对于溶解度受温度影响较大的物质,用降温结晶法提纯。②20℃时,甲的溶解度为40g,100g水中溶解了40g的甲,稀释前后溶质的质量相等,设稀释成质量分数为20%的溶液,应加水的质量为x,则40g=(100g+40g+x)×20%,解得x=60g,稀释在烧杯中进行,用到的仪器有玻璃棒、烧杯、100mL量筒、胶头滴管。(3)①水是一种最常见的溶剂。除去杂质的原则是不能引入新的杂质,根据流程图可知,第一步已经除去了氯化镁,所以第二步是将氯化钙转化为碳酸钙沉淀,Y是K2CO3。经过第二步除杂后,所含的杂质是K2CO3、KOH,此时加入过量的稀盐酸除去杂质,然后蒸发掉稀盐酸中的溶剂水、溶质氯化氢气体。③加入KOH溶液,是将MgCl2转化为沉淀除去,MgCl2+2KOH=Mg(OH)2↓+2KCl,两种化合物互相交换成分,生成另外两种化合物的反应是复分解反应。