题目内容
以下是某同学进行的两个实验探究
实验一:从含少量铜粉的银、锰(Mn)混合金属粉末中分离出贵金属,并获得一种盐晶体,将有关三种金属随意编号为:A、B、C,并设计了如下流程:
(1) A、B、C三种金属的活动性由强到弱的顺序为
(2)金属C是 ,操作a的名称是 。
(3)已知A的硫酸盐中A元素显+2价,请写出步骤①的反应的化学方程式: 。
实验二:研究镁条与稀盐酸反应过程中的能量变化以及反应速率的变化步骤:
⑴ 实验前需对镁条进行打磨,目的是 .
⑵ 检查图1装置的气密性。
⑶ 将镁条放入锥形瓶中,将注射器中的稀盐酸全部压入锥形瓶中,使之反应,发生反应的化学方程式为 。
⑷ 观察注射器活塞运动变化情况,绘制出注射器内收集到的气体体积变化与时间关系的图像如图2所示。则t1~t2时间内反应速率逐渐减慢的主要原因是 .
t2~t3时间内注射器内气体体积逐渐减少的原因 。
.实验一:(1) A>B>C ;(2) 银(Ag);结晶;(3) Mn+H2SO4 = MnSO4+H2↑;实验二 (1)去除镁条表面的氧化物薄膜;Mg+ 2HCl= MgCl2 + H2↑;稀盐酸的浓度逐渐减小,反应速率减慢 ;反应停止后温度降低,气体的体积减小。
解析试题分析:实验一:由题中的转化图可以知道(1) A、B、C三种金属的活动性由强到弱的顺序为A>B>C ;因为回收贵重金属,故金属C为银;操作a溶液中得到溶质,所以名称是结晶;(3)已知A的硫酸盐中A元素显+2价,步骤①的反应的化学方程式Mn+H2SO4 = MnSO4+H2↑;实验二:(1)实验前需对镁条进行打磨,目的是去除镁条表面的氧化物薄膜;⑶ 将镁条放入锥形瓶中,将注射器中的稀盐酸全部压入锥形瓶中,使之反应,发生反应的化学方程式为Mg+ 2HCl= MgCl2 + H2↑;(4)t1~t2时间内反应速率逐渐减慢的主要原因是稀盐酸的浓度逐渐减小,反应速率减慢;t2~t3时间内注射器内气体体积逐渐减少的原因反应停止后温度降低,气体的体积减小。
考点:物质的分离、金属活动性顺序、

化学实验是学习化学的重要方法.请完成下列金属性质的实验.
(1)实验一:比较铁、铜的金属活动性强弱.请你设计实验完成下表内容.
| 实验步骤 | 实验现象 | 结 论 |
| | | 金属活动性:Fe>Cu |
[实验]取一定量的镁、锌、铁三种金属分别加入到溶质质量分数相同的稀硫酸中,充分反应,观察现象.
[结论]活泼金属能与酸反应.
[分析]①三个反应的共同特点是 ,写出其中一个反应的化学方程式 .
②若完全反应后,三个反应生成氢气的质量相等,原因是 .
(8分)2014年央视 “3.15”晚会上曝出某品牌金饰品掺假的事件,引起同学们的好奇。小明同学拿来一片黄色的金属,和小军同学一起进行了相关探究活动。
【猜 想】①小明认为是黄金 ②小军认为是铜锌合金
【设计实验】
| 实验编号 | 实验操作 | 实验现象 |
| ① | 取一小片黄色金属放在石棉网上用酒精灯加热 | 黄色的金属变黑 |
| ② | 取一小片黄色的金属放入稀硫酸中 | |
(1)由实验①可知,猜想 (填序号)正确;写出反应的化学方程式
。
(2)实验②中的现象是 ,写出反应的化学方程式
。
【反思应用】假设你的观点和小军相同,请你选用一种类别不同于稀硫酸的试剂,再设计一个实验:取一小片黄色的金属放入 溶液中,实验中观察到的现象是 。
铁、铝、铜是常见的三种金属。同学们发现生活中的铝和铜制品表面一般不用防锈,而铁制品一般需要做防锈处理。
【提出问题】这是不是因为铁、铝、铜三种金属中铁的活动性最强呢?
【实验探究】同学们对这三种金属的活动性顺序展开了探究,请你参与探究并填写空格。
将粗细相同的铁丝、铝丝、铜丝分别插入体积相同、溶质质量分数也相同的稀盐酸中:
| 操作 | 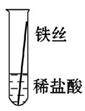 | 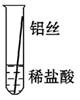 | 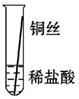 | 根据现象得出金属活动性顺序 |
| 片刻后现象 | 有少量气泡 | 无气泡 | 无气泡 | Fe>Al,Fe>Cu |
| 几分钟后现象 | 有少量气泡 | 有大量气泡 | 无气泡 | |
【讨论交流】为什么同一个实验得出了两种结论呢?同学们带着这个疑问查阅了相关资料,明白了铝丝在稀盐酸中短时间内无气泡,是因为铝表面致密的氧化膜会先与盐酸反应。
【反思评价】做金属性质实验时需将金属进行打磨,打磨的目的是________。
【实验验证】为了进一步确认铁、铝、铜这三种金属的活动性顺序,同学们又将两根粗细相同的、打磨过的铁丝分别插入硫酸铝溶液、硫酸铜溶液中:
| 操作 | 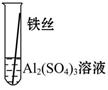 | 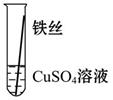 | 根据现象得出金属活动性顺序 |
| 现象 | 无明显现象 | | Al>Fe>Cu |
写出铁与硫酸铜溶液反应的化学方程式_________________。
【拓展迁移】(1)若只有一支盛有少量稀盐酸的试管,只需合理安排金属丝的插入顺序(能与盐酸反应的要一次将盐酸消耗完),也能证明铁、铝、铜这三种金属的活动性顺序。金属丝的插入顺序为________________。
(2)金属被人类大规模开发利用的大致年限也与金属活动性顺序有关,请写出铁、铝、铜三种金属材料被人类利用的先后顺序________________。




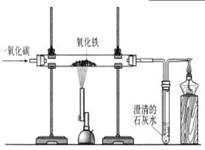

 H2SO4请写出该反应的化学方程式: .
H2SO4请写出该反应的化学方程式: .