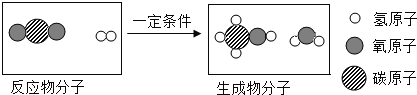
题目内容
【题目】某固体混合物可能含有BaCl2、FeCl3、Mg(NO3)2、Na2SO4、CaCO3中的一种或几种,为确定其组成,兴趣小组进行如下探究,请你参与解答相关问题。

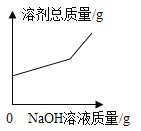
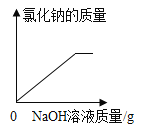
(1)分析图可知,固体混合物中不含有的物质是________。加入水后发生反应的化学方程式为____________
(提出问题)过滤所得无色溶液中含有哪些溶质?
(猜想与假设)猜想无色溶液中所含溶质可能为
猜想I: NaCl、Mg(NO3)2;
猜想II: NaCl、BaCl2;
猜想III: NaCl、Na2SO4;
猜想IV: NaCl、Mg(NO3)2、______
猜想V:含有NaCl、Mg(NO3)2、BaCl2。
(实验探究)
实验操作 | 实验现象 |
①取少量无色溶液于试管中,向其中滴加氢氧化钡溶液 | 产生白色沉淀 |
②在①反应后的试管中,加入足量的稀盐酸 | 白色沉淀部分溶解 |
(结论和反思)
(2)根据探究结果可知,猜想______成立, 步骤②沉淀溶解的化学方程式为_________
(3)若步骤②的现象为“白色沉淀全部溶解”,则该实验探究及步骤设计存在不足,因为这种情况下无法判断猜想_____和猜想_____哪个成立。
【答案】FeCl3(或氯化铁) ![]() Na2SO4 Ⅳ
Na2SO4 Ⅳ ![]() Ⅰ Ⅴ
Ⅰ Ⅴ
【解析】
(1)氯化铁溶液显黄色,可以推出溶质不含有氯化铁,加水后有沉淀生成,根据溶质组成沉淀组成可能为硫酸钡、碳酸钙中一种或两种,加入酸部分溶解,说明沉淀为混合物,氯化钡与硫酸钠反应生成硫酸钡沉淀和氯化钠,反应的化学方程式为![]() ;
;
猜想与假设:
无色溶液排除了氯化铁,硝酸镁无法判断是否存在,因此可在猜想中加入,若氯化钡与硫酸钠恰好反应,则溶质为氯化钠,或者是氯化钠与硝酸镁混合物,若氯化钡过量,则溶质为氯化钡、氯化钠,或者氯化钡、氯化钠与硝酸镁混合物,若硫酸钠过滤,则为氯化钠、硫酸钠或者氯化钠、硫酸钠与硝酸镁;
(2)无色溶液加入氢氧化钡,有白色沉淀生成,可能是氢氧化镁、硫酸钡,再加入盐酸,沉淀部分溶解,说明为氢氧化镁与硫酸钡混合物,因此确定硫酸钠和硝酸镁的存在,因此猜想Ⅳ正确;氢氧化镁与盐酸反应生成氯化镁和水,化学方程式为![]() ;
;
(3)白色沉淀全部溶解,说明沉淀中不含硫酸钡,则无色溶液中不含硫酸钠,该白色沉淀是氢氧化镁,说明有硝酸镁存在,至于氯化钡是否存在无法验证,因此Ⅰ和Ⅴ无法得出确切结论。