题目内容
【题目】海水晒盐提取食盐晶体后留下的母液叫卤水,卤水中除含NaCl外,还含有MgCl2、MgSO4等物质。它们的溶解度曲线如图所示。下列说法正确的是()
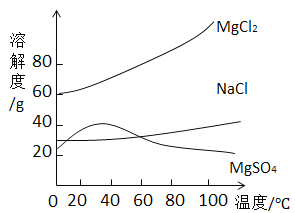
A.0℃时,三种物质的饱和溶液中,溶质质量分数最大的是MgSO4
B.三种物质的溶解度都随温度升高而不断增大
C.将卤水加热到80℃以上蒸发水分,逐渐析出的晶体是NaCl和MgSO4
D.20℃时,将40gNaCl固体和40gMgCl2固体中分别加入100g水充分溶解后,两种溶液均能达到饱和状态
【答案】C
【解析】
氯化镁的溶解度始终大于氯化钠的溶解度,硫酸镁的溶解度随温度升高先增大后变小。
A、0℃时,三种物质的饱和溶液中,溶质质量分数最大的是氯化镁,说法错误,不符合题意;
B、硫酸镁的溶解度随温度升高先增大后变小,说法错误,不符合题意;
C、氯化镁的溶解度受温度影响大,将卤水加热到80℃以上蒸发水分,逐渐析出的晶体是NaCl和MgSO4,氯化镁不易析出,说法正确,符合题意;
D、20℃时,氯化镁的溶解度大于40g,将40gNaCl固体和40gMgCl2固体中分别加入400g水充分溶解后,氯化镁不能达到饱和状态,说法错误,不符合题意。
故选C。

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案【题目】某同学查阅资料得知,实验室常用电石(主要成分CaC2)与水反应制取乙炔(C2H2),反应的化学方程式为:CaC2+H2O=Ca(OH)2+ C2H2![]() (电石中的杂质不溶于水且不参与反应)。在实验室中,该同学把一定量的CaC2加入Na2CO3溶液中,充分反应后过滤,得到滤渣和滤液,并对滤液的成分进行探究。
(电石中的杂质不溶于水且不参与反应)。在实验室中,该同学把一定量的CaC2加入Na2CO3溶液中,充分反应后过滤,得到滤渣和滤液,并对滤液的成分进行探究。
[提出问题]:滤液中溶质的成分是什么?
[猜想与假设]:猜想一:NaOH、Na2CO3
猜想二:NaOH
猜想三:NaOH、__________(将猜想三补充完整)
[分析与推理]:
反应后滤液中一定存在的溶质是__________(填化学式,下同),可能存在的溶质是______和______。对可能存在的溶质,需进一步实验验证。
[设计并实验]:
实验序号 | 实验操作 | 实验现象 | 实验结论 |
实验一 | 取少量滤液于试管中,向其中加入过量稀盐酸 | 无气泡产生 | 猜想_____不成立 |
实验二 | 另取少量滤液于试管中,向其中滴入适量碳酸钠溶液 | _________________ | 猜想三成立,发生反应的化学方程式为_______ |
[拓展延伸]:
若向CuCl2溶液中加入少量CaC2,充分反应,可观察到有气泡产生,同时出现蓝色的沉淀。写出产生蓝色沉淀的这一步反应方程式 ________________________。实验室保存电石应注意______。
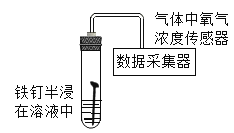
【题目】某研究小组为探究“铁钉在不同溶液中腐蚀的速率”,在相同条件下取同浓度的下列不同溶液用如图装置完成实验,并用手持数据采集器进行测定。回答下列问题:
所用溶液 | NH4Cl | (NH4)2SO4 | NH4NO3 |
0min时氧气浓度(%) | 20.8 | 20.8 | 20.8 |
500min时氧气浓度(%) | 15.8 | 17.0 | 17.4 |
实验前溶液PH | 5.31 | 5.53 | 5.50 |
实验后溶液PH | 7.37 | 7.99 | 8.22 |
铁钉表面锈蚀情况 | 大量铁锈 | 大量铁锈 | 大量铁锈 |
(1)用稀硫酸去除铁锈的化学反应方程式为_____
(2)在NH4Cl、(NH4)2SO4、和NH4NO3溶液中,铁钉锈蚀过程中上述溶液的酸性均变_____(填“强”或“弱”)
(3)上述实验方案是否合理?_____(填“合理”或“不合理”),你的理由是_____
(4)铁钉锈蚀的速率还可能与_____有关。请设计你的实验,验证你的猜想:
实验操作 | 实验现象及结论 |
_____ | _____ |
(注意:若答对第(5)小题奖励4分,化学试卷总分不超过60分)
(span>5)该小组在不同酸碱性溶液中又进行了探究,在相同条件下其测定的实验数据如下图:
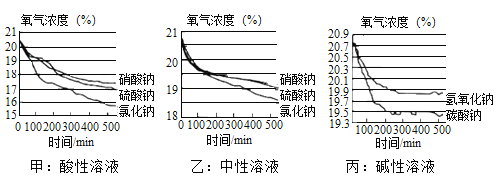
a、上述实验中,氧气浓度下降先陡后缓的原因为_____
b、根据甲、乙图像,请写出三点结论:
①结论:_____②结论:_____③结论:_____
【题目】小明同学在做铝和稀盐酸反应时无意中加入几滴硫酸铜溶液,发现铝片表面产生气泡速率明显增快,对此他产生了兴趣。
(提出问题)硫酸铜溶液是不是此反应的催化剂?硫酸铜溶液的体积对此实验有影响吗?
(设计并实验)室温下,小明将过量、表面积相同已打磨的铝片分别加入到6份30mL10%稀盐酸中,并在每份中加入不同体积的硫酸铜饱和溶液,记录获得相同体积氢气的时间,从而确定产生氢气的速率。
实验混合溶液 | 1 | 2 | 3 | 4 | 5 | 6 |
饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | 10 | 20 |
水/mL | 20 | 19.5 | 17.5 | V | 10 | 0 |
(1)上述表格中V=______________。
(2)写出铝和稀盐酸反应的化学方程式:______________。
(3)定量收集氢气体积可用如图________(填写字母序号)装置。
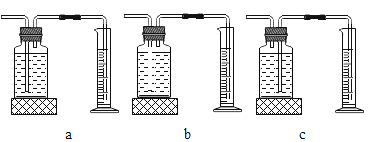
(实验现象)随着硫酸铜溶液体积的增加,产生氢气的速率先加快后明显减慢,且铝片表面附着的红色物质逐渐增加。
(结论与解释)
(4)随着硫酸铜溶液体积的增加,反应速率明显变慢可能的原因是___
(5)根据实验现象小明认为硫酸铜溶液不是此反应的催化剂,其原因是___
(实验反思)加速铝和稀盐酸反应速率还可以采取的措施是___(写出一点)
(注意:若正确回答下列各题奖励4分,化学总分不超过60分)
(实验拓展)根据上述实验,小明认为是盐中的金属离子影响了铝和稀盐酸的反应速率;为了研究不同金属离子对反应的影响,小明同学继续实验,取过量表面积相同的铝片和30mL10%稀盐酸混合后加入不同的盐溶液,实验现象如表(加号越多,代表反应速率越快):
实验1 | 实验2 | 实验3 | 实验4 | 实验5 | |
加入试剂0.5mL | 水 | 5%NaCl溶液 | 5%Mg2(NO)3溶液 | 5%FeSO4溶液 | 5%CuSO4溶液 |
产生气泡速率 | + | + | + | ++ | +++ |
(6)如表中,用水进行实验的目的是_________;
(7)上述实验设计存有缺陷,该缺陷是;改进实验后,仍符合上表中的实验现象,可得到的结论是:①______________;②______________.
【题目】实验室用石灰水而不用氢氧化钠溶液鉴定二氧化碳。氢氧化钠能否与二氧化碳反应?
【查阅资料】Ⅰ.氢氧化钠溶液与二氧化碳反应生成易溶的碳酸钠,碳酸钠在二氧化碳过量的条件下继续与水和二氧化碳反应生成碳酸氢钠
Ⅱ.碳酸钠和碳酸氢钠性质对比如下表
操作 | NaHCO3溶液 | Na2CO3溶液 |
加入稀盐酸 | 产生气泡 | 产生气泡 |
加入稀CaCl2溶液 | 无明显变化 | __________________(填写现象)) |
加热溶液至沸腾,并将气体通入澄清石灰水 | 澄清石灰水变浑浊 | 澄清石灰水无明显变化 |
【进行实验】
实验操作 | 实验现象 | 结论及化学方程式 |
| ___________________ | 氢氧化钠与二氧化碳反应生成碳酸钠.反应方程式_______________ |
【实验反思】学习小组讨论,认为产生此实验现象的原因可能有两种:一种是NaOH与C02发生了反应;另一种是_______________
(2)为了进一步验证CO2与NaOH溶液已经发生反应,请你设计一个简单的实验检验生成的新物质。
实验步骤 | 实验现象 | 解释与结论 |
____________________________ | ____________________________ | NaOH与CO2发生了反应 |
【实验拓展】该小组同学将二氧化碳通入氢氧化钠溶液中,利用数字化技术测定溶液pH值变化,待完全反应后,观察到溶液中逸出大量气泡,pH出现两段S型变化曲线。

【实验分析】
(3)AB段变化的原因可能是________。BC段变化的原因可能是___________。利用实验验证变化后的产物,实验操作为_________________.实验现象是____________________。