题目内容
海洋是个巨大的资源宝库,利用海水可制取许多化工产品.
(1)用海水制食盐,常通过______得到粗盐,粗盐中含有少量的CaCl2、Na2SO4等杂质. 除
去上述杂质,先加过量BaCl2溶液除去______,再加______溶液除去CaCl2和过 量的BaCl2,生成的沉淀经______除去.
(2)从海水中提取溴常用吹出法,即用氯气(Cl2)将海水里溴化钠(NaBr)中的溴置换出来,再用空气或水蒸气吹出溴(Br2).流程示意图如下:

①写出氯气置换出溴单质的化学方程式:______;该反应在pH=3的酸性条件下进行,可用______测定反应液的酸碱度.
②吹出的溴和大量空气混合在一起进入吸收塔(吸收塔中发生的反应:Br2+S02+2H20═H2S04+2HBr).根据流程图分析,通入S02的目的是______.
解:(1)海水晒盐的原理是通过蒸发海水制得粗盐,由于BaCl2可以和硫酸钠反应生成硫酸钡沉淀和氯化钠,以及碳酸钠可以和CaCl2反应生成氯化钠和碳酸钙除掉溶于水的杂质,同时由于生成的物质均是沉淀和氯化钠,所以过滤后溶液中只含有溶质氯化钠;
(2)依据题干叙述可知氯气和溴化钠可以置换出溴单质,其化学化学方程式为:Cl2+2NaBr=2NaCl+Br2,常见的测定溶液酸碱度的方法是使用pH试纸测定溶液的酸碱度,由于吸收塔中发生的反应是Br2+S02+2H20═H2S04+2HBr所以加入二氧化硫的目的是使溴与空气相互分离;
故答案为:(1)蒸发除水;Na2SO4;Na2CO3;过滤; (2)①Cl2+2NaBr=2NaCl+Br2;pH试纸 ②分离溴与空气;
分析:(1)依据海水晒盐的原理分析粗盐制得的方法,并依据BaCl2可以和硫酸钠反应以及碳酸钠可以和CaCl2反应生成氯化钠和碳酸钙除掉溶于水的杂质;
(2)依据题干叙述书写氯气置换出溴单质的化学方程式,并根据常见的测定溶液酸碱度的方法测定溶液的酸碱度,依据吸收塔中发生的反应分析加入二氧化硫的目的;
点评:此题是对海水相关问题的探讨,涉及到海水中杂质的除掉方法和原理,解题的关键是掌握溶液中杂质除掉的反应原理以及题干中有关信息使用.
(2)依据题干叙述可知氯气和溴化钠可以置换出溴单质,其化学化学方程式为:Cl2+2NaBr=2NaCl+Br2,常见的测定溶液酸碱度的方法是使用pH试纸测定溶液的酸碱度,由于吸收塔中发生的反应是Br2+S02+2H20═H2S04+2HBr所以加入二氧化硫的目的是使溴与空气相互分离;
故答案为:(1)蒸发除水;Na2SO4;Na2CO3;过滤; (2)①Cl2+2NaBr=2NaCl+Br2;pH试纸 ②分离溴与空气;
分析:(1)依据海水晒盐的原理分析粗盐制得的方法,并依据BaCl2可以和硫酸钠反应以及碳酸钠可以和CaCl2反应生成氯化钠和碳酸钙除掉溶于水的杂质;
(2)依据题干叙述书写氯气置换出溴单质的化学方程式,并根据常见的测定溶液酸碱度的方法测定溶液的酸碱度,依据吸收塔中发生的反应分析加入二氧化硫的目的;
点评:此题是对海水相关问题的探讨,涉及到海水中杂质的除掉方法和原理,解题的关键是掌握溶液中杂质除掉的反应原理以及题干中有关信息使用.

练习册系列答案
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
海洋是个巨大的资源宝库,它不仅孕育着无数的生命,还含有大量的化学物质.Ⅰ.海水制溴.从海水中提取的溴约占世界溴产量的1/3,工业上常用“吹出法”制溴,其工艺流程如下: 试回答:
试回答:
(1)步骤②中的化学方程式为2NaBr+Cl2=2NaCl+Br2,其反应类型是 .
(2)非金属单质也具有类似金属与盐溶液之间的反应规律,如在溶液中可发生下列反应:Cl2+2KBr=2KCl+Br2
Br2+2KI=2KBr+I2,由此可判断C12、I2、Br2活动性由强到弱顺序是 .
Ⅱ.食盐制碱.我国著名化学家侯德榜发明的联合制碱法的主要过程是:①向浓氨水中通入足量的二氧化碳生成碳酸氢铵溶液;②然后向溶液中加入食盐细粒充分搅拌,控制条件,利用物质的性质不同,两者发生反应生成碳酸氢钠.便有品体析出;③将析出的碳酸氢钠加热制得碳酸钠、二氧化碳和水.
四种盐在不同温度下的溶解度表:
请回答:
(3)过程①中发生反应的化学方程式 ,该反应类型 .
(4)根据溶解度表分析过程②中能发生反应的原因是 ,过程②发生的化学方程式 该反应的类型为 .
(5)过程③中反应的化学方程式是 .
 试回答:
试回答:(1)步骤②中的化学方程式为2NaBr+Cl2=2NaCl+Br2,其反应类型是
(2)非金属单质也具有类似金属与盐溶液之间的反应规律,如在溶液中可发生下列反应:Cl2+2KBr=2KCl+Br2
Br2+2KI=2KBr+I2,由此可判断C12、I2、Br2活动性由强到弱顺序是
Ⅱ.食盐制碱.我国著名化学家侯德榜发明的联合制碱法的主要过程是:①向浓氨水中通入足量的二氧化碳生成碳酸氢铵溶液;②然后向溶液中加入食盐细粒充分搅拌,控制条件,利用物质的性质不同,两者发生反应生成碳酸氢钠.便有品体析出;③将析出的碳酸氢钠加热制得碳酸钠、二氧化碳和水.
四种盐在不同温度下的溶解度表:
| 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | |
| 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| 碳酸氢铵 | 15.8 | 21.0 | 27.0 | ||
| 碳酸氢钠 | 8.1 | 9.6 | 11.1 | 12.7 | |
| 氯化铵 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
(3)过程①中发生反应的化学方程式
(4)根据溶解度表分析过程②中能发生反应的原因是
(5)过程③中反应的化学方程式是
海洋是个巨大的资源宝库,它不仅孕育着无数的生命,还含有大量的化学物质.
I.海水提溴.从海水中提取的溴约占世界溴产量的
,工业上常用“吹出法”制溴,其工艺流程如下:
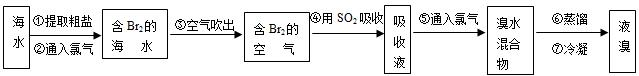
试回答:
(1)步骤②中的化学方程式为2NaBr+Cl2=2NaCl+Br2,其反应类型是 ,
(2)非金属单质也具有类似金属与盐溶液之间的反应规律,如在溶液中可发生下列反应:Cl2+2KBr=2KCl+Br2Br2+2KI=2KBr2+I2
由此可判断Cl2、I2、Br2活动性由强到弱顺序是 .
Ⅱ.食盐制碱.我国著名化学家侯德榜发明的联合制碱法的主要过程是:①向浓氨水中通人足量的二氧化碳生成碳酸氢铵溶液;②然后向溶液中加入食盐细粒充分搅拌,控制条件,利用物质的性质不同,两者发生反应生成碳酸氢钠,便有晶体析出;③将析出的碳酸氢钠加热制得碳酸钠、二氧化碳和水.
四种盐在不同温度下的溶解度表:
请回答:
(1)碳酸氢铵的化学式是 .
(2)由上表分析过程②中能发生反应的原因是 .
(3)过程③中反应的化学方程式是 .
I.海水提溴.从海水中提取的溴约占世界溴产量的
| 1 |
| 3 |

试回答:
(1)步骤②中的化学方程式为2NaBr+Cl2=2NaCl+Br2,其反应类型是
(2)非金属单质也具有类似金属与盐溶液之间的反应规律,如在溶液中可发生下列反应:Cl2+2KBr=2KCl+Br2Br2+2KI=2KBr2+I2
由此可判断Cl2、I2、Br2活动性由强到弱顺序是
Ⅱ.食盐制碱.我国著名化学家侯德榜发明的联合制碱法的主要过程是:①向浓氨水中通人足量的二氧化碳生成碳酸氢铵溶液;②然后向溶液中加入食盐细粒充分搅拌,控制条件,利用物质的性质不同,两者发生反应生成碳酸氢钠,便有晶体析出;③将析出的碳酸氢钠加热制得碳酸钠、二氧化碳和水.
四种盐在不同温度下的溶解度表:
| 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | |
| 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| 碳酸氢铵 | 15.8 | 21.0 | 27.0 | ||
| 碳酸氢钠 | 8.1 | 9.6 | 11.1 | 12.7 | |
| 氯化铵 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
(1)碳酸氢铵的化学式是
(2)由上表分析过程②中能发生反应的原因是
(3)过程③中反应的化学方程式是



