题目内容
【题目】如图是a、b、c三种物质的溶解度曲线,下列说法正确的是
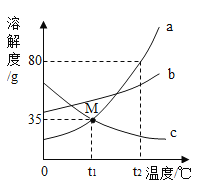
A. t1℃时a的饱和溶液,升温到t2℃时仍为饱和溶液
B. 降温可以使c的不饱和溶液变为饱和溶液
C. t1℃时,a和c的溶解度相等
D. t2℃时,在100g水中加入80gb能形成180g溶液
【答案】C
【解析】
A. a物质溶解度随温度的升高而增大,t1℃时a的饱和溶液,升温到t2℃时为不饱和溶液,说法错误;
B. a物质溶解度随温度的降低而增大,降温不可以使c的不饱和溶液变为饱和溶液,说法错误;
C. t1℃时,a和c的溶解度曲线相交,此时a和c的溶解度相等,说法正确;
D. t2℃时,b物质的溶解度小于80,在100g水中加入80gb物质,b物质不能全部溶解,不能形成180g溶液,说法错误。
故选:C。

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案【题目】化学小组在老师的指导下,在实验室用氨气(NH3)、二氧化碳和饱和氯化钠溶液等原料制 取小苏打(NaHCO3),制取流程如下图所示。
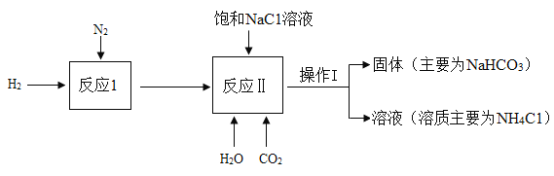
(1)“反应 I”是在高温、高压及催化剂存在的条件下发生的一种化合反应,目的是制取 “反应 II”所需的氨气。其化学方程式为_________。
(2)“操作 I”所需的玻璃仪器:_________。
(3)“反应 II”的条件不同,NaHCO3 产量不一样。不同条件下获取 NaHCO3 的部分数据 如下表所示:
标号 | 反应温度/℃ | 反应时间/min | NaHCO3产率/% |
a | 30 | 60 | 86.8 |
b | 30 | 120 | X |
c | 35 | 60 | 89.4 |
d | 35 | 120 | 92.5 |
e | 40 | 60 | 85.3 |
f | 40 | 120 | 85.6 |
①X 的数值可能是_________(填标号)。
A 85.8 B 86.8 C 92.1 D 93.1
②查阅文献获知,“反应 II”存在以下两个反应: NH3+CO2+H2O=NH4HCO3 NH4HCO3+NaCl=NaHCO3 ↓+NH4Cl,分析在相同反应时间,40℃时碳酸氢钠的产率比 35℃时低的可能原因:___________
(4)副产品 NH4Cl 可用于生产 NH3。一定条件下,氧化镁和 NH4Cl 反应可获取高产率的NH3 和另外两种化合物,这两种化合物的化学式分别为_________和_________。
【题目】实验室常用的干燥剂有浓硫酸、碱石灰(CaO和NaOH的固体混合物)等,后者在潮湿的空气中易变质。某化学兴趣小组对实验室中一瓶久置的碱石灰展开探究。
[查阅资料]①碱石灰易吸收空气中的水蒸气和二氧化碳 ②氯化钙溶液呈中性,碳酸钠溶液呈碱性 ③碳酸钠和氢氧化钙溶于水温度变化不明显 ④Ca(OH)2分解温度为580℃,CaCO3分解温度为825℃,Na2CO3的分解温度为1744℃。
[提出问题]碱石灰是否变质?其成分可能有哪些?
[进行猜想]①若没有变质,碱石灰吸水性良好,成分只有CaO和NaOH;
②若变质,该碱石灰中可能含有CaO、NaOH、Ca(OH)2、Na2CO3、CaCO3中的两种或两种以上。
[实验过程]
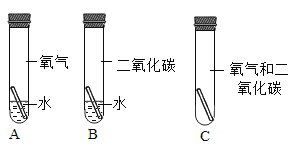
(1)验证碱石灰是否变质:图中的B为干燥装置,常用于固体干燥剂干燥气体。现用A、B装置检验碱石灰是否变质,取适量的无水硫酸铜和碱石灰样品分别装入A、B中,连接好A、B装置,从 ____(填“c”或“d”)端向B中缓缓通入水蒸气,观察A装置中的现象为____,证明碱石灰已变质。
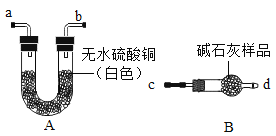
(2)验证碱石灰是否完全变质:取适量碱石灰样品放入试管中,加入足量蒸馏水使其充分溶解,溶液变浑浊,用手触摸试管外壁,温度无明显变化,证明碱石灰已完全变质。则样品成分最多有___种可能性(填数字)。
(3)为进一步确定碱石灰样品的成分,该小组继续实验并记录如下:
实验编号 | 实验操作 | 实验目的、现象或数据 | 实验结论 |
实验一 | ①取适量样品于试管中,加入足量蒸馏水使其充分溶解; ②过滤,得到滤渣A和滤液B;③向滤液B中加入足量CaCl2溶液,静置; ④________。 | 操作③的主要目的是:___ 操作④的现象:____ | 样品中一定有Ca(OH)2 |
实验二 | ①取干燥样品50g,控制在600℃内,加热至质量不再发生变化,冷却后称量; ②将①中剩余固体控制在850℃内反复加热,冷却后称量。 | 操作①中称得固体质量为45.5g;操作②固体质量无变化。 | 样品中一定没有_____(填化学式) |
[探究结论] 通过整个探究活动分析得知碱石灰样品的成分是______(填化学式),其中盐的质量分数为_____。
[反思与评价] 通过探究活动,大家知道该碱石灰变质的化学反应过程,其中生成盐的化学方程式为______;明白了碱石灰要密封保存的原因。
【题目】信息加工素养指学生在短时间内自学新知识,能对信息进行提取和加工的能力
(资料)
◎我国的酸雨因大量燃绕含硫量高的煤面形成,机动车排放的尾气也是重要成因
◎溶液的酸碱度常pH来表示,pH值是一个介于0和14之间的数,在25℃下,当pH<7时溶液呈酸性,数值越小酸性越强:当pH>7时,溶液呈碱性,数值越大碱性越强;当pH=7时,溶液呈中性。
(实验)某化学课外活动小组取刚降到地面的雨水水样,用pH计(测pH的仪器)每隔5分钟测一次pH,其数据如表所示,请回答下列问题
测定时刻 | 17:05 | 17:10 | 17:15 | 7:20 | 7:25 | 17:30 | 17:35 |
pH | 4.95 | 4.94 | 4.94 | 4.88 | 4.86 | 4.85 | 4.85 |
(1)在测定期间,该雨水为____________(填“酸性”“碱性”“中性”),而且逐渐________(填“增强”、减弱”或“不变”)
(2)若在17:40时刻测定,pH应为____________(填字母)
A 4.87 B 4.86 C 4.84 D 4.00
(应用)
(3)请提出一条减少酸雨的措施________________________
(4)回收二氧化硫可以生产硫酸,化学方程式为2SO2+O2+2H2O=2H2SO4,参加反应的SO2与生成的H2SO4的质量比是____________。若将3.2t的S完全燃烧,全部转化,可得到H2SO4的质量为____________t。