题目内容
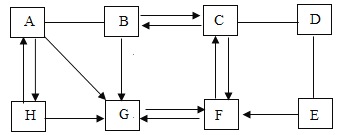
【题目】现欲探究一固体混合物A的成分,已知其中可能含有CuCl2、NH4NO3、(NH4)2SO4、CuO四种物质中的两种或多种。按图所示进行实验,出现的现象如图所示(设过程中所有可能发生的反应均恰好完全反应)。试根据实验过程和发生的现象填写以下空白:

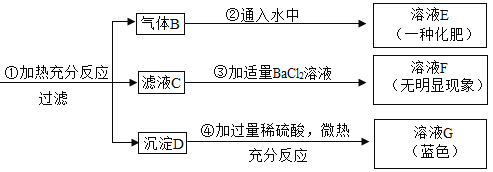
(1)产生的气体B的气味为_______________。
(2)溶液G中,一定存在的溶质是________________。
(3)混合物A中,肯定存在的物质是_________________。
(4)写出过程①中一定发生的化学反应的方程式是___________
(5)固体混合物里,上述四种物质中,还不能确定存在的物质是____________,得此结论的理由_______。
(6)为了进一步确定(5)中物质是否存在,请你简要写出实验方案_______(包括操作、现象和结论)。
【答案】有刺激性气味 硫酸铜和稀硫酸 硝酸铵和氧化铜 ![]() 氯化铜 氯化铜与氢氧化钠反应生成的氢氧化铜和硫酸也能反应生成蓝色溶液 向一只烧杯中加入适量的原固体混合物,加入足量的水充分溶解,若溶液为蓝色,则原固体中含有CuCl2;若溶液为无色,则原固体中不含有CuCl2
氯化铜 氯化铜与氢氧化钠反应生成的氢氧化铜和硫酸也能反应生成蓝色溶液 向一只烧杯中加入适量的原固体混合物,加入足量的水充分溶解,若溶液为蓝色,则原固体中含有CuCl2;若溶液为无色,则原固体中不含有CuCl2
【解析】
氢氧化铜和硫酸反应生成硫酸铜和水,氧化铜和硫酸反应需要微热生成硫酸铜和水,硝酸铵和氢氧化钠生成硝酸钠、水和氨气,氯化铜与氢氧化钠反应生成氢氧化铜和氯化钠。
(1)固体混合物加入氢氧化钠溶液有气体产生,则是固体中含有铵态氮肥,与氢氧化钠反应生成了有刺激性气味的氨气,故产生的气体B的气味为有刺激性气味。
(2)沉淀D能与硫酸反应生成蓝色溶液,则D中一定含有含铜元素,氢氧化铜和硫酸不需要加热反应即可快速进行,而氧化铜和硫酸反应需要微热才能进行,生成硫酸铜,加入的是过量的稀硫酸,故溶液G中,一定存在的溶质是硫酸铜和稀硫酸。
(3)固体混合物加入氢氧化钠溶液有气体产生,则是固体中含有铵态氮肥,与氢氧化钠反应生成了有刺激性气味的氨气,说明固体中含有硝酸铵或是硫酸铵;滤液C中加入氯化钡溶液没有明显的现象,说明不含有C中不含有硫酸根离子,即固体中不含有硫酸铵,一定含有硝酸铵;沉淀D能与硫酸反应生成蓝色溶液,则D中一定含有含铜元素,氢氧化铜和硫酸不需要加热反应即可快速进行,而氧化铜和硫酸反应需要微热才能进行,反应需要微热,含有的是氧化铜,D中可能含有氢氧化铜,原混合物中可能含有氯化铜,故混合物A中,肯定存在的物质是硝酸铵和氧化铜。
(4)过程①中一定发生的化学反应是硝酸铵和氢氧化钠生成硝酸钠、水和氨气,反应的化学方程式是![]() 。
。
(5)氯化铜与氢氧化钠反应生成氢氧化铜和氯化钠,氢氧化铜和硫酸反应生成硫酸铜和水,故固体混合物里,上述四种物质中,还不能确定存在的物质是氯化铜,得此结论的理由是氯化铜与氢氧化钠反应生成的氢氧化铜和硫酸也能反应生成蓝色溶液。
(6)要确定氯化铜是否存在,氯化铜的水溶液为蓝色进行,可以将固体混合物溶于水,观察所形成的溶液是否是蓝色进行,故实验方案是向一只烧杯中加入适量的原固体混合物,加入足量的水充分溶解,若溶液为蓝色,则原固体中含有CuCl2;若溶液为无色,则原固体中不含有CuCl2。

【题目】某工厂排故的废水中含有AgNO3、Cu(NO3)2和Al(NO3)3,某校化学兴趣小组的同学取了一瓶废水样品带回实验室进行实验.将废水静置后,取上层清液,加入锌粉.待充分反应后,得到固体A和溶液B.由图可知,操作a的名称是______.
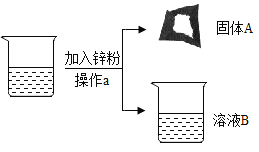
化学兴趣小组的同学对固体A的成分进行了探究,请你一起参与(不考虑杂质干扰)
(提出问题)固体A的成分是什么?
(猜想与假设)甲同学认为固体A是银;乙同学认为固体A是银和铜;丙同学认为固体A是银、铜、铝,你认为固体A还可能是______.
大家经过讨论后,认为丙同学的猜想错误,理由是______.
(实验探究)设计实验探究固体A的成分,请填写表中空白:
实验步骤 | 现象 |
实验1:取固体A加入盐酸 | 无气体产生 |
实验2:取溶液B加入_____ | 无蓝色沉淀 |
由实验可知,固体A一定是______.
(反思交流)若实验1观察到下列现象:固体A![]() 无色气体,则溶液B中溶质的成分为______;写出产生气体反应的化学方程式______.
无色气体,则溶液B中溶质的成分为______;写出产生气体反应的化学方程式______.