题目内容
【题目】某兴趣小组计划对空气成分进行探究,以下是他们的实验设计方案:
![]()
(1)除去二氧化碳和水蒸气:装置和操作步骤略。
(2)除去氧气:该小组根据教材中拉瓦锡研究空气成分的实验原理,除去了(1)中得到的气体中的氧气。在拉瓦锡的经典实验中(装置如图),使用汞的优点有_______。
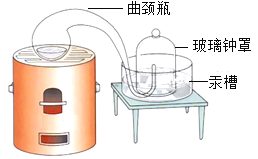
A 汞为液态,在加热的条件下只与氧气反应且生成物为固体
B 时间足够长,能将密闭装置中的氧气几乎耗尽
C 无法观察装置中气体体积的变化
(3)分析误差:该小组按设计方案得到的氮气密度(假设要除去的气体均已除净)与氮气的实际密度有误差,产生误差的原因是_______。
(4)拓展与延伸:实验室如何制取氮气呢?请阅读资料并回答下列问题:
资料:
1.重铬酸铵为橘黄色粉末,加热至180![]() 时可分解得到氮气;
时可分解得到氮气;
2.氮气的化学性质不活泼,常温下很难跟其他物质发生反应。但在高温或点燃条件下可与某些物质反应,如:镁能够在氮气中燃烧。
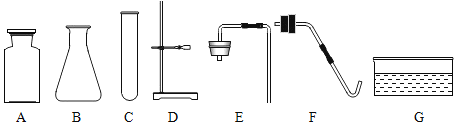
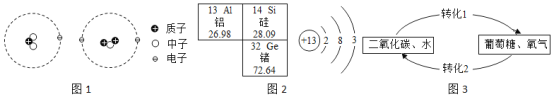
①仪器B的名称是______。
②利用上述仪器和重铬酸铵在实验室制取少量氮气,其发生装置应选择的仪器有_____(填序号),还必须补充的一种仪器是_____。若用上述装置制氧气,反应的化学方程式为____。
③根据已有知识,收集氮气只能用____法,理由是______。该小组欲进行镁在氮气中的燃烧实验,现收集一瓶含水约1/5体积的氮气,该如何操作______。
【答案】AB 得到的气体中还含有稀有气体 锥形瓶 CDF 酒精灯 2KMnO4![]() K2MnO4+MnO2+O2↑(2KClO3
K2MnO4+MnO2+O2↑(2KClO3![]() 2KCl+3O2↑) 排水法 氮气密度接近空气且难溶于水 向集气瓶中装满水,倒扣入水槽中;当收集到约剩余1/5体积水时,停止收集;盖上毛玻璃片后移出集气瓶,放在实验台上
2KCl+3O2↑) 排水法 氮气密度接近空气且难溶于水 向集气瓶中装满水,倒扣入水槽中;当收集到约剩余1/5体积水时,停止收集;盖上毛玻璃片后移出集气瓶,放在实验台上
【解析】
(2)除去氧气,装置如图2,使用汞的优点有:A.汞为液态,在加热的条件下只与氧气反应且生成物为固体;B.时间足够长,能将密闭装置中的氧气几乎耗尽;故答案为:AB;
(3)分析误差:该小组按设计方案得到的氮气密度(假设要除去的气体均已除净)与氮气的实际密度有误差,产生误差的原因是:得到的气体中还含有稀有气体;故答案为:得到的气体中还含有稀有气体;
(4)拓展与延伸,①仪器B的名称是锥形瓶;②利用上述仪器和重铬酸铵在实验室制取少量氮气,需要加热,其发生装置应选择固体加热型装置,选择的仪器有:CDF,还必须补充的一种仪器是:酒精灯;如果是高锰酸钾或氯酸钾制氧气也需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,氯酸钾在二氧化锰的催化下受热分解生成氯化钾和氧气;③氮气的密度比空气略小,难溶于水,因此只能用排水法收集;该小组欲进行镁在氮气中的燃烧实验,现收集一瓶含水约1/5体积的氮气,操作是:向集气瓶中装满水,倒扣入水槽中;当收集到约剩余1/5体积水时,停止收集,盖上毛玻璃片后移出集气瓶,放在实验台上。
故答案为:①锥形瓶; ②CDF;酒精灯;2KMnO4![]() K2MnO4+MnO2+O2↑(2KClO3
K2MnO4+MnO2+O2↑(2KClO3![]() 2KCl+3O2↑);③排水; 氮气密度接近空气且难溶于水;向集气瓶中装满水,倒扣入水槽中;当收集到约剩余1/5体积水时,停止收集,盖上毛玻璃片后移出集气瓶,放在实验台上。
2KCl+3O2↑);③排水; 氮气密度接近空气且难溶于水;向集气瓶中装满水,倒扣入水槽中;当收集到约剩余1/5体积水时,停止收集,盖上毛玻璃片后移出集气瓶,放在实验台上。

【题目】某化学兴趣小组为了测定粗锌中锌的质量分数,在10g粗锌中分5次共加入50.0g稀硫酸(杂质不与硫酸反应),部分数据如下表所示,请计算:
容器中硫酸的质量/g | 10 | 20 | 40 | 50 |
气体质量/g | 0.1 | 0.2 | m | 0.3 |
(1)当加入40g硫酸时,对应的气体质量m是___________g。
(2)粗锌中锌的质量_______________________。