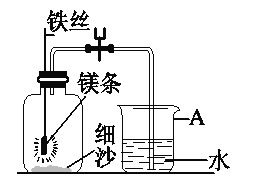
题目内容
【题目】水是维系生命的重要物质.之一,天然水需净化才能饮用,下图是水厂净化水的过程:
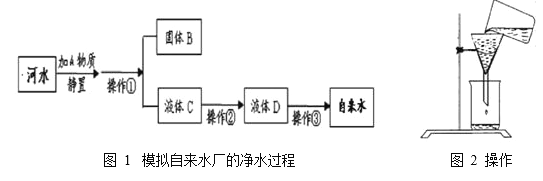
(1)下列属于该自来水厂净水方法的是____________(填字母序号);
A.沉淀 B.过滤 C.消毒 D.蒸馏
(2)经过自来水厂净化后的水属于_______________(填“纯净物”或“混合物”);
(3)国家新版《生活饮用水卫生标准》从2012年7月1日起全面实施,其中消毒剂除氯气以外,同时补充了一氯胺(NH2Cl)、二氧化氯、臭氧(O3)三种物质,其中二氧化氯的化学式为 _____________;
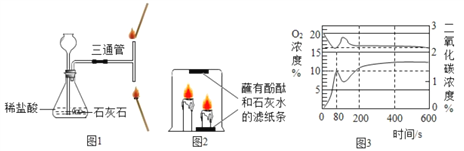
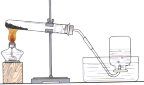
(4)小刚收集到一瓶浑浊的河水,他要模拟自来水厂的净水过程,最终制成自来水。其实验过程如下所示,请回答以下问题。
I : 图 1 中操作①的名称是 ________,在该操作中,小刚操作如图 2 所示,请你写出其中两处明显的错误:① ________________② ___________________;
II :图1操作②常用活性炭来除去一些异味和色素,这是利用活性炭的 __________性;
III:小刚发现经净化后的液体D 是硬水,要降低水的硬度,日常生活中可以采用的方法是: ________。
【答案】A B C 混合物 ClO2 过滤 没有用玻璃棒引流 漏斗下端没有紧贴烧杯内壁(或漏斗内液面高于滤纸边缘) 吸附 煮沸
【解析】
(1)根据自来水厂净水常用的方法分析判断;
(2)根据自来水厂净化后水的组成分析;
(3)根据物质的名称写出化学式;
(4)I、根据过滤操作分析;II、根据活性炭的作用分析;III、根据硬水软化的方法分析。
(1)自来水厂生产自来水时,常用的净水方法有沉淀、过滤、吸附、消毒等,所以,ABC正确;
(2)自来水厂净化后的水中含有可溶性的物质,属于混合物;
(3)二氧化氯的化学式为:ClO2;
(4)I、过滤是把不溶于液体的固体与液体分离的一种方法,经过操作①得到了固体和液体,故操作①是过滤;该操作中用到玻璃棒引流,同时图中漏斗下端没有紧贴烧杯内壁,漏斗内液面高于滤纸边缘;
II、活性炭具有吸附性,能吸附除去一些异味和色素;
III、硬水是指含有较多的钙、镁离子化合物的水,生活中常用煮沸的方法来降低水的硬度。

 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案【题目】研究和控制化学反应条件有重要意义。
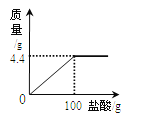
(1)同学们想探究过氧化氢的浓度对反应速率的影响。在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间。
实验 | 30%双氧水 的质量(g) | 加入的水 的体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
1 | 10 | 20 | 5 | 200 |
2 | 20 | 20 | 5 | 100 |
3 | 30 | 20 | ______________ | 67 |
①取用二氧化锰的仪器是 ______。
②二氧化锰在过氧化氢的分解中起_________作用。
③实验3中,加入的二氧化锰质量为_________g。
④相同条件下,实验3产生氧气的速率最快,说明_________。
(2)同学通过查阅资料得知,过氧化氢在70℃以上会较快分解产生氧气。为了验证加热过氧化氢也可以产生氧气,同学们选择右图装置(气密性良好)进行实验。实验中观察试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是___________,同学分析原因后,采用了______法收集气体,再检验,证明加热双氧水也可产生氧气。