题目内容
【题目】(6分)现有家庭食用碱样品12g(主要成分Na2CO3,其它成分不与酸反应),向其中加入某未知浓度的盐酸,生成气体的质量与加入盐酸的质量关系如图。请计算:
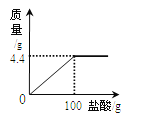
(1)食用碱中碳酸钠的纯度是多少?
(2)盐酸的溶质的质量分数是多少?
(要求写出计算过程,结果精确到0.1)
【答案】(1)88.3%(2)7.3%
【解析】
试题分析:解:设食用碱中碳酸钠的质量为x,参与反应的HCl质量为y。
Na2CO3 + 2HCl = 2NaCl + CO2 ↑ + H2O
106 73 44
x y 4.4g
列比例式得:106:X=73:Y=44:40克
求得 X =10.6 g y = 7. 3 g
(1)碳酸钠的纯度 = 10.6克/12 ×100% = 88.3%
(2)盐酸的溶质质量分数 = 7.3克/100克 ×100%=7.3%

练习册系列答案
相关题目