题目内容
【题目】已知A、B为两种黑色粉末,D为红色金属.C、F都是无色气体,A、B、C、D、E、F五种物质之间的转化关系如图所示.(部分生成物已省略)请回答:
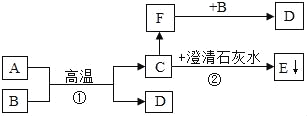
(1)B的化学式为_____;D的化学式为_____.
(2)反应①的基本反应类型是_____;反应②的化学方程式为_____;在上述反应中A、F都具有_____性.
(3)将两只用于医学研究的小白鼠分别放入盛放C、F的两个瓶中,拧紧瓶盖,结果两只小白鼠很快都死了.造成小白鼠死亡的主要原因_____(填“相同”或“不同”).
【答案】(1)CuO; Cu
(2)置换反应;CO2+Ca(OH)2="==CaCO3↓+H2O" ;还原
(3)不同
【解析】
根据题干提供的信息进行分析解答,D为红色金属,故D是铜,黑色粉末A、B 反应生成铜和能使石灰水变浑浊的C,故C为二氧化碳,A和B是碳和氧化铜,二氧化碳转化生成F,F能与B反应生成铜,故F是一氧化碳,B是氧化铜,A是碳,E是碳酸钙,据此解答.
D为红色金属,故D是铜,黑色粉末AB 反应生成铜和能使石灰水变浑浊的C,故C为二氧化碳,A和B是碳和氧化铜,二氧化碳转化生成F,F能与B反应生成铜,故F是一氧化碳,B是氧化铜,A是碳,E是碳酸钙,带入框图,推断合理;
(1)B是氧化铜,D是铜,故填:CuO;Cu
(2)碳能与氧化铜高温反应生成铜和二氧化碳,是单质与化合物反应生成单质和化合物,属于置换反应;二氧化碳能与氢氧化钙反应生成碳酸钙沉淀和水;A是碳,F是一氧化碳,都具有还原性,故填:置换反应;Ca(OH)2+CO2═CaCO3↓+H2O;还原
(3)C是二氧化碳,不能帮助呼吸,本身无毒,而F是一氧化碳,是有毒的气体,故造成小白鼠死亡的原因不同,故填:不同

【题目】某化学兴趣小组用实验室常用药品(或溶液)对“NaOH溶液与稀盐酸是否恰好完全反应”进行探究。
(知识卡片):氯化钠溶液显中性。氯化铜易溶于水。
(实验探究):
(1)方案Ⅰ:某同学先向试管中加入约2mLNaOH溶液,再滴入几滴酚酞溶液,溶液变红。然后慢慢滴入稀盐酸,边滴边振荡,直至溶液恰好变为无色。
①实验结论_________。
②从微观的角度分析,该反应的实质是_________。
③在滴入稀盐酸的过程中,若观察到有少量气泡出现,请分析产生气泡的可能原因_______(用化学方程式表示)。
(2)方案Ⅱ:
实验步骤 | 实验现象 | 结论 |
取2mLNaOH溶液于试管中,滴入一定量的稀盐酸,振荡后加入镁条 | 若_______ | 稀盐酸过量 |
若没有明显现象 | NaOH溶液与稀盐酸恰好完全反应 |
(实验反思):
(3)另有同学提出方案Ⅱ不能证明NaOH溶液与稀盐酸恰好完全反应,其原因是______。
(4)除以上方案外,下列哪些物质单独使用,也能证明“NaOH 溶液与稀盐酸是否恰好完全反应”_________ (填序号)。
A 铜片 B pH试纸 C 氧化铜 D 紫色石蕊试液
【题目】现有铜与金属X组成的混合物粉末,金属X是镁、铁、锌中的一种.利用该混合物进行如下实验:
实验步骤及数据:取该混合物粉末8.0g放入烧杯中,将140.0g 溶质质量分数为14.0%的稀硫酸平均分四次加入该烧杯中,充分反应后,测得烧杯内剩余固体的质量数据如下表:
加入稀硫酸的次数 | 第1次 | 第2次 | 第3次 | 第4次 |
烧杯内剩余固体质量/g | 6.8 | 5.6 | 4.4 | 4.2 |
实验通过计算,求:
(1)该混合物粉末中铜的质量分数为_____;
(2)该混合物是由铜粉和_____组成的;
(3)第三次加入硫酸充分反应后,所得溶液中溶质的质量分数是多少?_____(写出计算过程)
(4)若用溶质的质量分数为98%、密度为1.84g/cm﹣3的浓硫酸来配制本实验中所用的稀硫酸,则需要取浓硫酸多少毫升?_____同时加入水多少毫升?_____(写出计算过程)