题目内容
【题目】某粗盐中除NaCl以外还含有少量杂质MgCl2,为了测定粗盐中MgCl2的质量分数。取固体样品50.0g完全溶解于150.0g水中,并向其中逐渐加入一定浓度的NaOH溶液,实验过程中生成沉淀的质量与加入NaOH溶液的质量的关系如图所示:

注:发生反应的化学方程式为:MgCl2+2NaOH=Mg(OH)2↓+2NaCl
请根据相关信息完成下列计算:
(1)反应完全时,生成氢氧化镁的质量为_____g;
(2)在粗盐中氯化镁的质量分数;_____
(3)恰好完全反应时得到的溶液中溶质的质量分数。_____
【答案】![]() 19.0% 17.4%
19.0% 17.4%
【解析】
解析根据图示可知,生成的氢氧化镁的质量为5.8g,根据氢氧化镁的质量以及反应的化学方程式即可计算出氯化的质量和生成的氯化钠的质量,进而可求出粗盐中氯化镁的质量分数以及恰好完全反应时得到的溶液中溶质的质量分数。
(1)由图可知生成的氢氧化镁的质量为![]()
(2)设样品中![]() 的质量为 x,生成NaCl的质量为y。
的质量为 x,生成NaCl的质量为y。
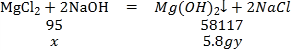
![]()
![]()
x=9.5g y=11.7g
![]() 的质量分数
的质量分数![]()
(3)反应后所得溶液中NaCl的质量分数![]()
答:![]() 反应完全时,生成氢氧化镁的质量为
反应完全时,生成氢氧化镁的质量为 ![]() ;
;
![]() 样品中
样品中![]() 的质量分数为
的质量分数为![]() ;
;
![]() 反应后所得溶液中NaCl的质量分数为
反应后所得溶液中NaCl的质量分数为![]() 。
。

练习册系列答案
相关题目