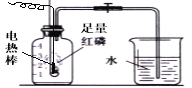
题目内容
【题目】黄铜矿经初步处理后,所得溶液甲中的溶质为Fe2(SO4)3、CuSO4及H2SO4,利用以下实验可制取补血剂原料碳酸亚铁并回收铜。
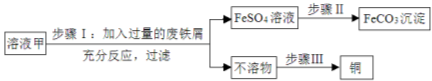
(1)步骤Ⅰ中,发生反应的化学方程式包括:
①Fe2(SO4)3+Fe 3FeSO4 ,
② ,
③ 。
(2)步骤Ⅱ中加入一种试剂可实现其转化,该试剂可以是 (填化学式)。
(3)步骤Ⅲ回收铜的实验操作包括:①过滤、②洗涤、③加足量稀硫酸、④干燥,正确的操作排序是 (填序号)。
(4)若废铁屑含有少量铁锈,对实验结果 (填“有”或“无”)影响。
【答案】(1)Fe+H2SO4 FeSO4+H2↑ Fe+CuSO4 FeSO4+Cu
(2)Na2CO3 (3)③①②④ (4) 无
【解析】
试题分析:步骤Ⅰ中,发生反应的化学方程式包括: Fe2(SO4)3+Fe 3FeSO4 ,Fe+H2SO4 FeSO4+H2↑ Fe+CuSO4 FeSO4+Cu;步骤Ⅱ中加入一种试剂可实现其转化,该试剂可以是Na2CO3,碳酸钠和硫酸亚铁发生反应变为碳酸亚铁沉淀和硫酸钠。步骤Ⅲ回收铜的实验操作包括:③加足量稀硫酸、①过滤、②洗涤、④干燥,先加入酸,将铁完全除掉。若废铁屑含有少量铁锈,对实验结果无影响。

【题目】实验室利用下图实验装置进行有关化学实验,请回答下列问题:

(1)写出图中指定仪器的名称:① ;② 。
(2)实验室用氯酸钾和二氧化锰制取氧气,发生装置可选择图中的 (填字母),该反应的化学方程式为: 。
(3)某同学想通过装置C收集二氧化碳,气体应从 (填“a”或“b”)进入。
(4)对上述制取二氧化碳实验后的固液残留物进行分离,可选择上图中的装置 (填字母),该操作中玻璃棒的作用是 。
(5)某水泥厂化验室,为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水。)有关实验数据如下表:
反应前 | 充分反应后 | ||
实验 数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
180 g | 12g | 187.6g | |
求该石灰石中碳酸钙的质量分数。(计算结果保留一位小数)