题目内容
【题目】某化学兴趣小组根据下图所示装置进行实验室制取气体的探究.回答下列问题:

(1)写出图中编号仪器名称:b ;
(2)用高锰酸钾制氧气的化学方程式为 ,生成的两种固体,一种易溶于水的钾盐,一种难溶于水的黑色氧化物,可以采用加水、溶解、 (操作名称),回收后利用装置 (字母序号)作为过氧化氢制氧气的催化剂。
(3)若用石灰石和稀盐酸制取和收集干燥的二氧化碳,应选择的装置组合为 (填字母),制取二氧化碳的化学方程式为 .
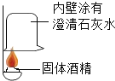
(4)下图装置可用来测量生成的CO2气体的体积,其中在水面上放一层植物油的目的是 ,植物油上方原有的空气对实验的结果 (填“有”或“没有”)明显影响.

【答案】(1)b长颈漏斗; (2)2KMnO4==== △ K2MnO4 + MnO2 + O2↑,过滤,B
(3)BFE 、CaCO3+2HCl = CaCl2+H2O+CO2↑(4)防止CO2气体溶于水中,导致测量不准确,没有
【解析】
试题分析:(2)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4![]() K2MnO4+MnO2+O2↑;难溶于水的黑色氧化物可以过滤回收;
K2MnO4+MnO2+O2↑;难溶于水的黑色氧化物可以过滤回收;
(3)用石灰石和稀盐酸制取CO2是固液常温型,收集干燥的二氧化碳,必加个干燥装置,且密度大于空气,故组合为BFE;方程式为CaCO3+2HCl = CaCl2+H2O+CO2↑;
(4)要测量二氧化碳口体积只能用排水法,用量筒测量水口体积从而测二氧化碳口体积;二氧化碳能溶于水,所以要在水口上方放一层植物油.植物油上方原有口空气不会溶解在水中,所以油上方口空气对实验结果没有影响.

 阅读快车系列答案
阅读快车系列答案【题目】小强在回家的途中经过一鱼塘边时,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙(CaO2),请你与小强共同探究。
(1)为研究鱼塘中大量气泡是何种气体所致,小强使用如下图所示的装置进行实验,打开仪器a的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃,说明生成的气体是 。由此可知养鱼师傅向鱼塘中撒过氧化钙的目的是 ,仪器a的名称是 。

(2)根据质量守恒定律,小强认为过氧化钙与过量水反应还应产生某种含有钙元素的产物。开始小强假设该产物为CaO,但通过思考他很快否定了原先的假设,并重新假设生成的含钙产物为Ca(OH) 2。请解释小强否定原假设建立新假设的理由: 。
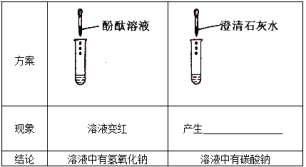
请设计一个实验方案来验证小强的新假设,并填入下表空格中:
实验步骤 | 可能出现的现象 | 结论 |
CaO2与H2O反应有Ca(OH) 2生成 | ||
CaO2与H2O反应无Ca(OH) 2 生成 |
(3)小强通过实验证明了过氧化钙与水反应的确有氢氧化钙生成,请写出过氧化钙和水反应的化学方程式: 。
(4)小强在实验时观察到烧杯中有气泡产生,由此他还得出了什么结论 。