题目内容
【题目】某化学兴趣小组欲采用不同的方法配制硫酸铜溶液,请回答问题:
(1)小君用溶解硫酸铜固体的方法配制100g8%硫酸铜溶液,具体步骤如下:
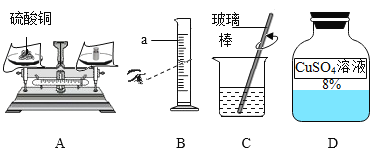
Ⅰ.计算。需要硫酸铜固体的质量为_____g。
Ⅱ.称量。
①称量过程中,若发现天平指针偏右,此时应该(填字母)_____,至指针指向标尺中央。
A 调节游码和砝码 B 调节平衡螺母 C 减少硫酸铜固体 D 增加硫酸铜固体
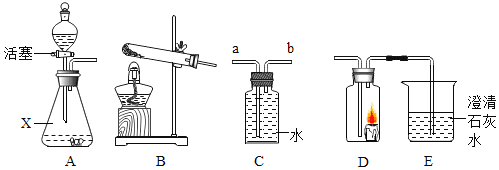
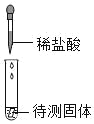
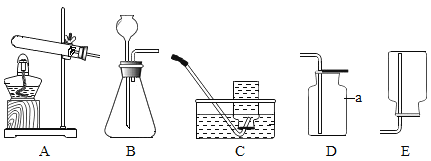
②量取水时,如果按照图B的方法读数,会使配制的溶液溶质质量分数_____(填“偏大”或“偏小”)。
Ⅲ.溶解。
Ⅳ.装瓶,贴标签。
(2)小东用溶液稀释的办法配制100g8%硫酸铜溶液,需要20%的硫酸铜溶液(密度为1.16g/mL)的体积为_____mL(列出计算式即可),需要加入的水的体积为_____mL。
【答案】8 D 偏小 ![]() 60
60
【解析】
Ⅰ.计算。溶液质量与溶质质量分数的乘积是溶质的质量,则需要硫酸铜固体的质量为100g×8%=8g;
Ⅱ.称量。
①称量过程中,若发现天平指针偏右,应增加硫酸铜固体。故选D。
②量筒读数时视线应与液体凹液面最低处相平,量取液体时仰视读数,实际量取体积多于读数,加入溶剂质量增大,溶质质量分数减小;
(2)设需要20%的硫酸铜溶液(密度为1.16g/mL)的体积为为x。稀释前后溶质质量不变,100g×8%=x×1.16g/mL×20%,可得x=![]() ,≈34.5mL;需要加入的水的体积为(100g-100g×8%÷20%)÷1g/mL=60mL;
,≈34.5mL;需要加入的水的体积为(100g-100g×8%÷20%)÷1g/mL=60mL;

练习册系列答案
相关题目
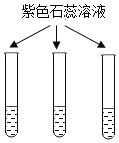
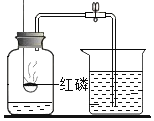
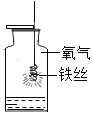
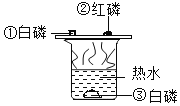
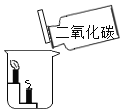
【题目】对下图所示实验现象进行分析得出的结论中,错误的是( )
|
|
|
|
A.氧气约占空气体积的1/5 | B.铁丝能在氧气中燃烧 | C.②③对比说明物质燃烧需要氧气 | D.二氧化碳的密度比空气大,不燃烧也不支持燃烧 |
A.AB.BC.CD.D